Hội chứng ổ khuyết (lacunar syndomes) là một biểu hiện lâm sàng của đột quỵ não ổ khuyết (lacunar infarctions), là một trong những nguyên nhân đột quỵ não thường gặp nhất ở bệnh nhân tăng huyết áp hệ thống mạn tính. Các ổ khuyết này thường hình thành do sự tắc nghẽn các mạch máu nhỏ trong não, gây ra sự thiếu máu và tổn thương các tế bào não. Tổng quan về Hội chứng ổ khuyết cho thấy đây là một bệnh lý thường gặp và có thể gây ra những hậu quả nghiêm trọng cho sức khỏe của người bệnh. Tuy nhiên, với việc chẩn đoán và điều trị đúng cách, bệnh nhân có thể phục hồi và giảm thiểu các triệu chứng của bệnh.
Bài viết trích nguồn từ Hội thần kinh học Việt Nam
Tác giả:
Nguyễn Thị Hường1, Nguyễn Thanh Bình2
Bệnh viện Đa khoa Quốc tế Vinmec Times City1
Đại học Y Hà Nội2
1. Định nghĩa và lịch sử
Đột quỵ não ổ khuyết được định nghĩa là những ổ tổn thương nhỏ dưới vỏ có đường kính dưới 15mm do tắc các tiểu động mạch hoặc động mạch xiên (penetrating arteries) là những nhánh tách trực tiếp từ các động mạch não lớn, thường gặp nhất là từ đa giác Willis, động mạch não giữa và động mạch nền. Các động mạch xiên là những mạch máu có kích thước nhỏ hơn 0.5mm đường kính, kích thước của một ổ nhồi máu tối đa từ 0.5 – 15mm tương đương với một thể tích 0.2 – 2ml. Cần lưu ý rằng không phải tất cả các nhồi máu nhỏ ở sâu đều là nhồi máu ổ khuyết. Chẩn đoán nhồi máu ổ khuyết đòi hỏi phải loại trừ các nguyên nhân nhồi máu não khác.
Thuật ngữ “lacune” lần đầu được Dechambre sử dụng vào năm 1838 dựa trên các phân tích sinh bệnh học của ông về các tổn thương dưới vỏ trên bệnh phẩm sinh thiết não [1]. Ở thời điểm đó, người ta cho rằng nguyên nhân của những tổn thương “lacune” hoặc là do viêm, hoặc là tổn thương chảy máu thoái triển, hoặc hoại tử sau nhồi máu. Marie năm 1901 mô tả một hội chứng lâm sàng với nhiều ổ “lacune”, bao gồm liệt nửa người với khả năng hồi phục tốt, rối loạn dáng đi bước nhỏ đặc trưng (dáng đi bước nhỏ Dejerine – marche a petis pas de Dejerine), liệt giả hành và sa sút trí tuệ. Năm 1960, Fisher nhờ những phân tích tỉ mỉ về mối tương quan lâm sàng và bệnh học đã đưa ra “học thuyết lacunar”, gợi ý rằng “lacune” là hậu quả của bệnh lý mạch máu mạn tính liên quan tới tăng huyết áp, với biểu hiện lâm sàng đa dạng và tiên lượng hồi phục tốt [2].
Từ đầu thế kỷ 20, những quan niệm mới về “lacune” đã được đưa ra và gây nhiều tranh cãi trong việc sử dụng thuật ngữ cũng như xác định bệnh nguyên và bệnh sinh. Người ta thấy rằng sự hình thành các khoang nhỏ trong nhu mô không phải do nguồn gốc thiếu máu mà do sự giãn rộng các khoang quanh mạch (etat criblé), đôi khi là di chứng của các vi chảy máu. Do đó trong thực hành lâm sàng ta nên phân biệt hai thuật ngữ sau:
Ổ khuyết (lacune) hoặc nhồi máu ổ khuyết (lacunar infarction) dùng để chỉ các ổ nhồi máu nhỏ < 15mm, khu trú trong sâu, có hoặc không có triệu chứng xác định, là tổn thương gây ra bởi một bệnh mạch máu nhỏ, cục bộ, đặc biệt xảy ra ở người có tiền sử tăng huyết áp mạn tính và không có các bệnh lý khác có thể gây ra tổn thương này.
Nhồi máu nhỏ ở sâu (pettit infarctus profond): lâm sàng và chẩn đoán hình ảnh chỉ ra một tổn thương có như trên nhưng do một nguyên nhân khác gây ra mà không phải bệnh lý mạch máu nhỏ.
2. Dịch tễ
Đột quỵ não ổ khuyết chiếm khoảng 15 – 26% số trường hợp nhồi máu não. Theo dữ liệu gánh nặng bệnh tật toàn cầu (GBD) năm 2016, ước tính nguy cơ đột quỵ gần như tương đương giữa nam và nữ giới, nguy cơ suốt đời là 18.3% với đột quỵ thiếu máu não cục bộ và 8.2% với chảy máu não [3]. Trong một nghiên cứu cộng đồng, tỷ lệ nhồi máu não ổ khuyết trong cộng đồng người da trắng là 29 trên 100.000 dân, trong khi tỷ lệ này ở người da đen là 52 trên 100.000 dân [4]. Như đa số quy mô dịch tễ của các nguyên nhân nhồi máu não khác, tỷ lệ đột quỵ não ổ khuyết tăng lên theo tuổi. Tỷ lệ bệnh nhân nhồi máu não ổ khuyết có sa sút trí tuệ tăng gấp 4 – 12 lần dân số chung [5]. Sa sút trí tuệ sau nhồi máu ổ khuyết thường gặp mặc dù các ổ nhồi máu não nhỏ có liên quan tới bệnh mạch máu nhỏ. Ngoài ra nhồi máu não ổ khuyết xảy ra ở người càng lớn tuổi thì càng dễ dẫn đến tình trạng tàn tật lâu dài nặng hơn.
3. Bệnh sinh đột quỵ não ổ khuyết
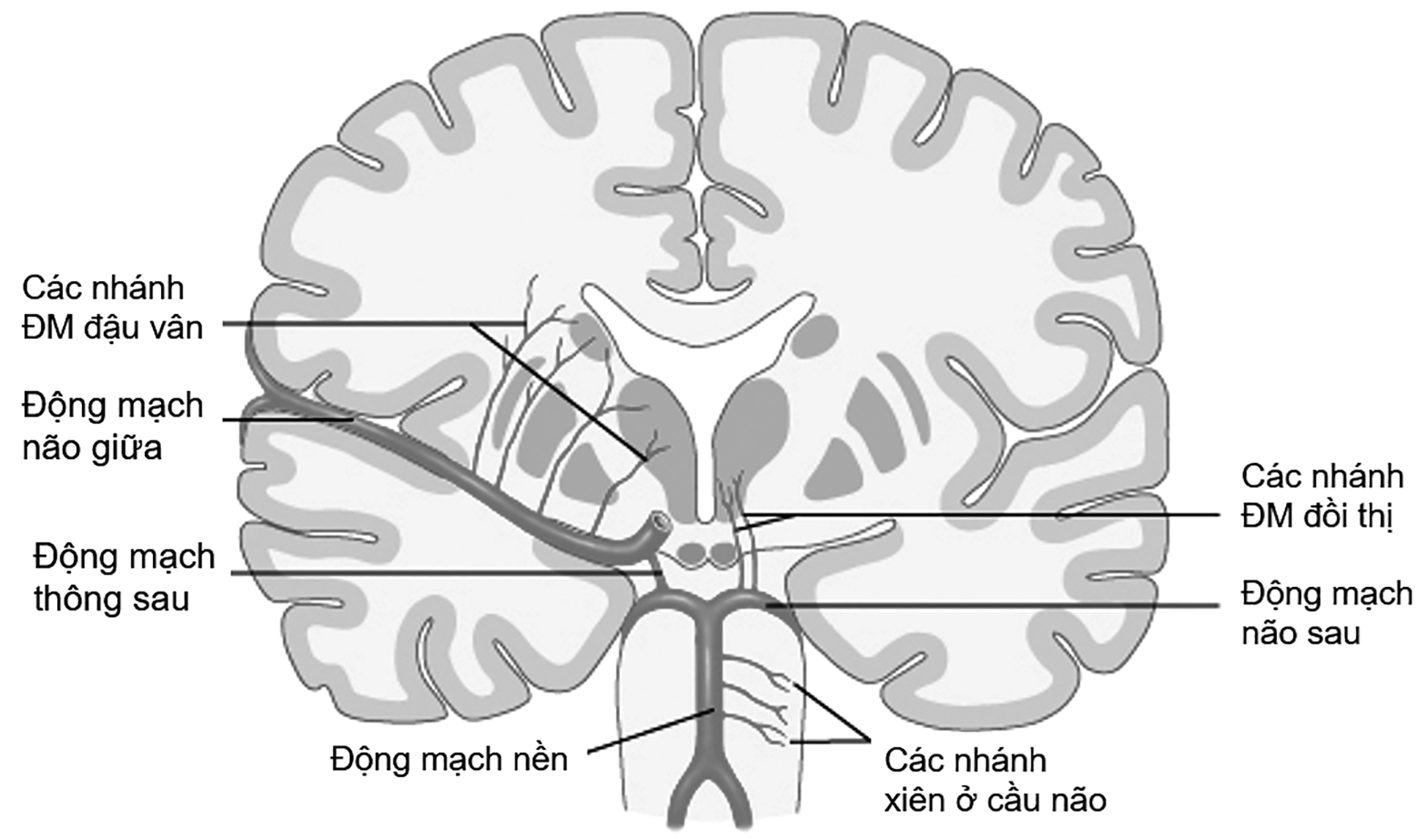
Hầu hết đột quỵ não ổ khuyết xảy ra ở các nhân nền, đồi thị, chất trắng dưới vỏ (bao trong, vành tia), và cầu não. Vị trí nhồi máu thuộc diện cấp máu của các động mạch xiên, là các nhánh động mạch đậu vân (nhánh của động mạch não giữa), động mạch quặt ngược Heubner (nhánh của động mạch não trước), động mạch mạch mạc trước (nhánh của động mạch cảnh trong), các nhánh động mạch đồi thị (nhánh của động mạch não sau), các nhánh xiên ở cầu não của động mạch nền [6] [7]. Các nhánh này tách ra trực tiếp từ các động mạch não lớn, do vậy chúng đặc biệt dễ bị tổn thương do tác động của tăng huyết áp. Sự nối thông thưa thớt và chồng lấn tối thiểu trong diện cấp máu của các nhánh xiên lý giải nguyên nhân ổ khuyết thường gặp với nhồi máu những khu vực này. Các cơ chế bệnh sinh của đột quỵ não ổ khuyết đã được thống nhất, bao gồm:
Bệnh vi mạch tăng huyết áp (microangiopathy): tăng huyết áp mạn tính không được kiểm soát dẫn đến dày thành động mạch, gây hẹp lòng các nhánh động mạch xiên, liên quan đến thoái hóa mỡ – kính (lipohyalinosis – thoái hóa lớp áo giữa của thành động mạch nhỏ và thay thế bằng lipid và collagen), hoại tử fibrin và loạn sản thành mạch [8] [9] [10].
Xơ vữa mạch nhánh (brach atheromatous disease): hình thành các vi xơ vữa tại các nhánh của động mạch não giữa, đa giác Willis, động mạch thân nền và đốt sống [11]
Huyết khối (embolism) nguồn gốc từ hẹp mạch cảnh do xơ vữa hoặc từ tim [12] [13] [14].
Rối loạn chức năng nội mô và tổn thương hàng rào máu não: giả thuyết cho rằng sự rối loạn chức năng nội mô động mạch và mao mạch hàng rào máu não dẫn đến phù quanh mạch, tổn thương tế bào thành mạch và thần kinh đệm, hình thành bệnh mạch máu nhỏ, nhồi máu não ổ khuyết và tổn thương chất trắng [15] [16].
Hình 1. Giải phẫu các động mạch não và nhánh xiên của chúng
Yếu tố nguy cơ của đột quỵ não ổ khuyết liên quan đến bệnh mạch máu mạn tính do tăng huyết áp hệ thống (tăng huyết áp và đái tháo đường). Giới tính nam, tuổi cao, hút thuốc lá, TIA hoặc nhồi máu não ổ khuyết trước đó và bệnh mạch vành cũng là những yếu tố nguy cơ. Ngoài ra yếu tố gen cũng được xem xét. Một nghiên cứu tổng quan năm 2021 đã chỉ ra 12 locus có liên quan đến đột quỵ não ổ khuyết [17]. Bệnh lý mạch máu nhỏ di truyền cũng có biểu hiện lâm sàng nhồi máu ổ khuyết bao gồm: bệnh mạch máu não dạng bột, CADASIL (bệnh động mạch di truyền trội nhiễm sắc thể kèm nhồi máu dưới vỏ và bệnh não chất trắng), CARASIL (bệnh động mạch di truyền lặn nhiễm sắc thể kèm nhồi máu dưới vỏ và bệnh não chất trắng).
4. Đặc điểm lâm sàng các hội chứng ổ khuyết thường gặp
Đa số các đột quỵ não ổ khuyết là không có triệu chứng. Hội chứng ổ khuyết là biểu hiện lâm sàng của các tổn thương tại những vị trí nhất định kể trên. Cho đến nay, có hơn 20 hội chứng ổ khuyết đã được mô tả trong y văn, tuy nhiên năm hội chứng ổ khuyết sau đây đã được công nhận rộng rãi (các hội chứng ổ khuyết cổ điển):
– Liệt vận động nửa người đơn thuần (Pure motor hemiparesis)
– Đột quỵ não cảm giác đơn thuần (Pure sensory stroke)
– Đột quỵ não vận động – cảm giác (Sensorimotor stroke)
– Liệt nửa người thất điều (Ataxic hemiparesis)
– Hội chứng nói khó – bàn tay vụng về (Dysarthria – clumsy hand syndrome)
Do tổn thương vị trí dưới vỏ, nhìn chung trong hội chứng ổ khuyết sẽ có sự vắng mặt các triệu chứng biểu hiện tổn thương vỏ não như thất ngôn, bán manh, rối loạn nhận thức, mất nhận thức nửa người, … Ngoài ra, nhồi máu não ổ khuyết là thể nhồi máu thường gặp nhất xuất hiện tình trạng thiếu hụt vận động nặng hơn sau nhập viện, triệu chứng tiến triển từ vài giờ đến vài ngày do tính chất tắc mạch từng nấc (stepwise). Bệnh nhân với bệnh mạch máu nhỏ tăng huyết áp có nguy cơ hình thành nhiều ổ tổn thương dưới vỏ dạng ổ khuyết có hoặc không kèm theo tổn thương chất trắng, có thể dẫn tới sa sút trí tuệ mạch máu.
4.1. Liệt vận động nửa người đơn thuần
Liệt vận động nửa người đơn thuần là hội chứng ổ khuyết thường gặp nhất (45 – 57% các trường hợp) [18]. Nó được đặc trưng bởi biểu hiện liệt vận động tay, chân, mặt một bên kèm theo vắng mặt các triệu chứng vỏ não (thất ngôn, bán manh, rối loạn nhận thức, mất nhận thức nửa người) và thiếu hụt cảm giác. Triệu chứng liệt có thể hoàn toàn hoặc không hoàn toàn nhưng thường là đồng đều (50%), tay – mặt (29%), một chi (18%).
Tổn thương hay gặp ở bao trong nhưng cũng có thể ở các vị trí khác trên đường vỏ – tủy. Thiếu hụt vận động có thể xảy ra đơn độc hoặc sau các cơn TIA nửa người. Một loạt ca bệnh sau đó được mô tả như hội chứng “cảnh báo bao trong”, dự báo nhồi máu cấp bao trong trên CT sọ não. Một số có thể diễn tiến do thiếu máu cục bộ nhánh xiên do huyết khối xơ vữa mạch lớn (động mạch não giữa, động mạch nền) gây triệu chứng dao động vận động.
4.2. Đột quỵ não cảm giác đơn thuần
Chiếm khoảng 7 – 18% các trường hợp hội chứng ổ khuyết [18]. Thiếu hụt cảm giác với tê bì ở tay, chân và mặt một bên không kèm liệt và các triệu chứng vỏ não. Triệu chứng cảm giác có thể là cảm giác nông, sâu hoặc cả hai, có thể cục bộ (cầu não) hoặc nửa người (đồi thị).
4.3. Liệt nửa người thất điều
Đặc trưng bởi liệt nửa người kèm thất điều chi cùng bên, chiếm 3 – 18% các trường hợp hội chứng ổ khuyết [18]. Triệu chứng thất điều chi do sự xâm phạm bó vỏ – tiểu não gây quá tầm, mất liên động và giảm trương lực cơ. Một số bệnh nhân có thể biểu hiện nói khó, nystagmus, và rối loạn dáng đi lệch về bên bệnh. Như các hội chứng ổ khuyết khác, các triệu chứng vỏ não không có mặt.
4.4. Đột quỵ não vận động cảm giác
Biểu hiện liệt nửa người kèm tê bì mặt, tay, chân cùng bên không kèm triệu chứng vỏ não, chiếm 15 – 20% các trường hợp hội chứng ổ khuyết [18]. Nhồi máu tại vị trí sau bên đồi thị và cánh tay sau bao trong. Về lý thuyết, các động mạch xiên từ động mạch não sau cấp máu cho đồi thị trong khi các nhánh đậu vân của động mạch não giữa cấp máu cho bao trong, do đó vị trí động mạch thủ phạm trong nhồi máu ổ khuyết có thiếu hụt vận động cảm giác còn đang tranh cãi.
4.5. Hội chứng nói khó – bàn tay vụng về
Ít gặp nhất trong số các hội chứng ổ khuyết cổ điển, chỉ chiếm 2 – 6% [18]. Biểu hiện liệt mặt, nói khó (vừa đến nặng) và yếu nhẹ tay kèm vụng về, nhất là ở ngọn chi (rõ nhất khi viết), tăng phản xạ gân xương cùng bên và nuốt khó. Không có rối loạn cảm giác và các triệu chứng vỏ não.
| Hội chứng ổ khuyết cổ điển | Vị trí tổn thương | Biểu hiện lâm sàng | Giá trị chẩn đoán dương tính |
| Liệt vận động nửa người đơn thuần | Bao trong, vành tia, nền cầu não, hành não | Liệt mặt, tay, chân 1 bên, không có rối loạn cảm giác, nói khó có thể gặp | 52 – 85% |
| Đột quỵ não cảm giác đơn thuần | Đồi thị, trần cầu não, vành tia | Tê bì mặt, tay, chân 1 bên, không có liệt | 95 – 100% |
| Liệt nửa người thất điều | Bao trong, vành tia, nền cầu não, đồi thị | Liệt vận động và thất điều 1 bên | 59 – 95% |
| Đột quỵ não vận động cảm giác | Thalamocapsular, nền cầu não hoặc hành não bên | Liệt nửa người kèm thiếu hụt cảm giác cùng bên | 51 – 87% |
| Hội chứng nói khó bàn tay vụng về | Nền cầu não, bao trọng, vành tia | Liệt mặt 1 bên, nói khó với liệt nhẹ tay và vụng về | Khoảng 96% |
Các hội chứng ổ khuyết khác với biểu hiện lâm sàng đa dạng, một số do tắc mạch lớn, còn lại do nhồi máu ổ khuyết, nhiều hội chứng không chứng minh được do nhồi máu ổ khuyết nhưng cũng không bác bỏ được.
| Các hội chứng ổ khuyết khác | Vị trí tổn thương |
| Liệt vận động nửa người đơn thuần kèm thất ngôn vận động | Gối hoặc cánh tay trước bao trong, cạnh chất trắng vùng vành tia trước |
| Liệt vận động nửa người đơn thuần không kèm liệt mặt | Dải tháp ở hành não (động mạch đốt sống/nhánh của nó) |
| Hội chứng não giữa – đồi thị (liệt dây III, liệt liếc dọc (hội chứng Parinaud), giảm động lực) | Nhồi máu hình cánh bướm (butterfly shape) vùng cạnh giữa trung não, dưới đồi, đồi thị hai bên (tắc động mạch Percheron, động mạch cạnh giữa đồi – dưới đồi, động mạch cạnh giữa trung não) |
| Sa sút trí tuệ đồi thị (giảm động lực, mất trí nhớ, hội chứng Horner) | Trung tâm đồi thị và vùng dưới đồi lân cận (tắc động mạch cạnh giữa đồi – dưới đồi trước) |
| Liệt vận động nửa người đơn thuần kèm liệt liếc ngang | Nhồi máu cạnh giữa vùng cầu não thấp (hội chứng một và một nửa) |
| Liệt vận động nửa người đơn thuần kèm liệt dây III đối bên (hội chứng Weber) | Cạnh đường giữa cuống não, vị trí thoát ra của dây III |
| Liệt vận động nửa người đơn thuần kèm liệt dây VI đối bên | Cạnh đường giữa cầu não trước, vị trí thoát ra của dây VI |
| Liệt vận động nửa người đơn thuần kèm lú lẫn | Cánh tay trước và phần trước cánh tay sau bao trong bên phải |
| Thất điều tiểu não kèm liệt dây III đối bên (hội chứng Claude) | Dải răng đỏ (dentatorubral tract – cuống tiểu não trên), ngay sau khi bắt chéo |
| Múa vung nửa người | Thể Luys (dưới đồi) (động mạch não sau, động mạch thông sau, động mạch mạch mạc sau) |
| Hội chứng nhánh thấp động mạch nền – chóng mặt, rung giật nhãn cầu, nhìn đôi, liệt liếc ngang, liệt vận nhãn liên nhân, thất ngôn, thất điều tiểu não, tê bì mặt theo nhánh dây V | Trần cầu não (nhánh dưới của động mạch nền hoặc các nhánh trên của động mạch đốt sống) |
| Hội chứng hành não bên | Động mạch đốt sống, động mạch tiểu não sau dưới |
| Hội chứng hành – cầu não bên – chóng mặt, ù tai, nystagmus, liệt VII, thất điều tiểu não, hội chứng Horner, phân ly cảm giác | Các nhánh thấp của động mạch đốt sống, diện chi phối nhân dây VII và VIII |
| Hội chứng khóa trong (liệt vận động hai bên nửa người đơn thuần) | Ảnh hưởng dải vỏ tủy hai bên: bao trong, cầu não, dải tháp, cuống não |
| Trạng thái ổ khuyết (l’état lacunaire) – hội chứng giả hành tủy có hoặc không kèm theo sa sút trí tuệ mạch máu | Nhiều tổn thương ổ khuyết |
5. Chẩn đoán hình ảnh đột quỵ não ổ khuyết
Đột quỵ não ổ khuyết ở những vị trí nhất định dẫn đến các hội chứng đột quỵ não ổ khuyết khác nhau. Tương tự như vậy, một đột quỵ não không phải ổ khuyết và chảy máu não nhỏ có thể biểu hiện như hội chứng ổ khuyết, điều này nhấn mạnh sự cần thiết phải chẩn đoán hình ảnh – thần kinh thích hợp cho tất cả các bệnh nhân nghi ngờ đột quỵ não.
Nhồi máu não ổ khuyết được mô tả là những tổn thương dưới vỏ có kích thước < 15mm. Tuy nhiên, một vài nghiên cứu chẩn đoán hình ảnh trong giai đoạn cấp (<10 ngày từ khi khởi phát triệu chứng) đã xác định giới hạn kích thước của ổ khuyết là 20mm thậm chí 25mm trên xung DWI, vì theo thời gian đa phần các ổ tổn thương sẽ giảm thể tích. Như đã phân tích, không phải nhồi máu não nhỏ nào cũng là nhồi máu ổ khuyết và việc chẩn đoán nhồi máu ổ khuyết đòi hỏi loại trừ các nguyên nhân đột quỵ não khác.
CLVT sọ não là lựa chọn ban đầu cho hầu hết các bệnh nhân đột quỵ não cấp, tuy nhiên CLVT có độ nhạy thấp trong chẩn đoán nhồi máu ổ khuyết (30 – 44%) [19], thậm chí còn có thể thấp hơn trong pha tối cấp (< 6 giờ). CLVT cũng bị hạn chế trong việc xác định các nhồi máu cấp tính hố sau và nhồi máu vùng vỏ não. Do đó, thường quan sát thấy tổn thương ổ khuyết trên CLVT sọ não ở giai đoạn mạn tính. MRI sọ não khắc phục được phần nào những nhược điểm trên khi xác định được chính xác vị trí nhồi máu mới. Trên hình ảnh MRI, ổ nhồi máu não ổ khuyết được quan sát với tính chất giảm tín hiệu trên xung T1W, tăng tín hiệu trên xung T2W, hạn chế khuếch tán trên DWI. Độ nhạy của MRI là lớn nhất với thể liệt vận động nửa người đơn thuần với việc phát hiện tới 85% số tổn thương. MRI thường thấy được các tổn thương trong vòng 8 giờ kể từ khi khởi phát triệu chứng. Kích thước ổ tổn thương cấp tính trên DWI thường bị đánh giá cao hơn kích thước thực của ổ khuyết ở ngày thứ 30 khoảng 40% [20].
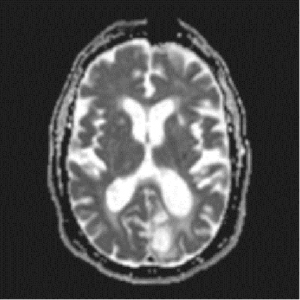
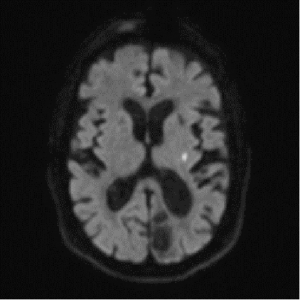
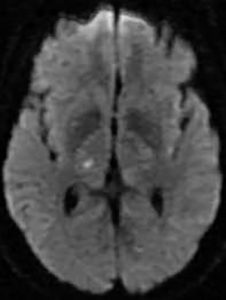
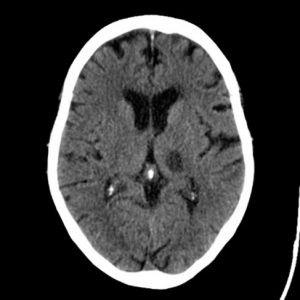
Hình 2. Hình ảnh học nhồi máu não ổ khuyết: (A) CLVT sau 24 giờ tổn thương giảm tỷ trọng đồi thị trái, bệnh nhân nữ 70 tuổi nhồi máu não ổ khuyết đồi thị trái; (B) MRI DWI tổn thương hạn chế khuếch tán đồi thị phải, bệnh nhân nam 70 tuổi nhồi máu não ổ khuyết đồi thị phải; (C) (D) MRI tổn thương hạn chế khuếch tán trên DWI và giảm tín hiệu trên ADC vị trí đồi thị trái, bệnh nhân nam 85 tuổi nhồi máu não ổ khuyết đồi thị trái.
6. Điều trị đột quỵ não ổ khuyết
Bệnh nhân đột quỵ não cấp đến sớm nên được đánh giá để trở thành ứng cử viên cho các liệu pháp điều trị tái thông, bao gồm tiêu sợi huyết đường tĩnh mạch và lấy huyết khối cơ học. Aspirin và các thuốc kháng kết tập tiểu cầu khác không nên được sử dụng trong vòng 24 giờ đầu sau tiêu sợi huyết. Tiêu sợi huyết có liên quan đến khoảng 6% các chảy máu não có triệu chứng, việc sử dụng nên được thảo luận kỹ với gia đình bệnh nhân. Mặt khác, nếu không có chống chỉ định, thuốc kháng kết tập tiểu cầu nên được khởi động càng sớm càng tốt khi chẩn đoán TIA hoặc nhồi máu não, thậm chí trước khi cơ chế chính xác của nhồi máu được xác định.
Trong dự phòng thứ phát đột quỵ não, bệnh nhân nên được điều trị nội khoa tích cực và kiểm soát yếu tố nguy cơ, bao gồm kiểm soát huyết áp, liệu pháp kháng kết tập tiểu cầu và statin, và điều chỉnh lối sống. Can thiệp này phù hợp cho cả bệnh nhân biểu hiện đột quỵ não/TIA và cả bệnh nhân không có tiền sử đột quỵ nhưng có nhồi máu não ổ khuyết trên hình ảnh học (nhồi máu não thầm lặng). Tuy nhiên, lợi ích và nguy cơ của liệu pháp kháng kết tập tiểu cầu chưa được nghiên cứu đầy đủ ở các bệnh nhân nhồi máu ổ khuyết thầm lặng.
Hiệu quả của aspirin và các liệu pháp kháng kết tập tiểu cầu khác trong dự phòng đột quỵ não thứ phát và tử vong đã được chứng minh ở các bệnh nhân đột quỵ não không do huyết khối từ tim nói chung. Một phân tích gộp năm 2015 đánh giá các liệu pháp kháng kết tập tiểu cầu so với placebo và báo cáo kết quả, trong dưới nhóm nhồi máu não ổ khuyết, điều trị liệu pháp kháng kết tập tiểu cầu đơn liên quan đến việc giảm đáng kể nguy cơ nhồi máu não tái phát (RR 0.48, 95% CI 0.30 – 0.78) [21]. Kết quả từ thử nghiệm SPS3 gợi ý việc sử dụng kháng kết tập tiểu cầu kép (phối hợp aspirin và clopidogrel) trong thời gian dài có thể có hại cho bệnh nhân đột quỵ não ổ khuyết do làm tăng nguy cơ xuất huyết và tử vong nhưng không làm giảm tỷ lệ nhồi máu tái phát [22].
TÀI LIỆU THAM KHẢO
1. Dechambre A. Mémoire sur la curabilité du ramollissement cérébral. Gaz Med Paris 1838; 6:305.
2. FISHER CM. LACUNES: SMALL, DEEP CEREBRAL INFARCTS. Neurology 1965; 15:774.
3. Gorelick PB. The global burden of stroke: persistent and disabling. Lancet Neurol 2019; 18(5):417-418.
4. Petty GW, Brown RD, Whisnant JP, Sicks JD, O’Fallon WM, Wiebers DO. Ischemic stroke subtypes: a population-based study of incidence and risk factors. Stroke 1999; 30(12):2513-6
5. Loeb C, Gandolfo C, Croce R, Conti M. Dementia associated with lacunar infarction. Stroke 1992; 23(9):1225-9.
6. Fisher CM. Capsular infarcts: the underlying vascular lesions. Arch Neurol 1979; 36:65.
7. Feekes JA, Hsu SW, Chaloupka JC, Cassell MD. Tertiary microvascular territories define lacunar infarcts in the basal ganglia. Ann Neurol 2005; 58:18.
8. Fisher CM. Lacunar strokes and infarcts: a review. Neurology 1982; 32:871.
9. Blevins BL, Vinters HV, Love S, et al. Brain arteriolosclerosis. Acta Neuropathol 2021; 141:1.
10. Pantoni L. Cerebral small vessel disease: from pathogenesis and clinical characteristics to therapeutic challenges. Lancet Neurol 2010; 9:689.
11. Caplan LR. Intracranial branch atheromatous disease: a neglected, understudied, and underused concept. Neurology 1989; 39:1246.
12. Macdonald RL, Kowalczuk A, Johns L. Emboli enter penetrating arteries of monkey brain in relation to their size. Stroke 1995; 26:1247.
13. Hart RG, Foster JW, Luther MF, Kanter MC. Stroke in infective endocarditis. Stroke 1990; 21:695.
14. Cacciatore A, Russo LS Jr. Lacunar infarction as an embolic complication of cardiac and arch angiography. Stroke 1991; 22:1603.
15. Wardlaw JM, Sandercock PA, Dennis MS, Starr J. Is breakdown of the blood-brain barrier responsible for lacunar stroke, leukoaraiosis, and dementia? Stroke 2003; 34:806.
16. Wardlaw JM. What causes lacunar stroke? J Neurol Neurosurg Psychiatry 2005; 76:617.
17. Traylor M, Persyn E, Tomppo L, et al. Genetic basis of lacunar stroke: a pooled analysis of individual patient data and genome-wide association studies. Lancet Neurol 2021; 20:351.
18. Chamorro A, Sacco RL, Mohr JP, et al. Clinical-computed tomographic correlations of lacunar infarction in the Stroke Data Bank. Stroke 1991; 22:175.
19. Hommel M, Besson G, Le Bas JF, et al. Prospective study of lacunar infarction using magnetic resonance imaging. Stroke 1990; 21:546.
20. Koch S, McClendon MS, Bhatia R. Imaging evolution of acute lacunar infarction: leukoariosis or lacune? Neurology 2011; 77:1091.
21. Kwok CS, Shoamanesh A, Copley HC, et al. Efficacy of antiplatelet therapy in secondary prevention following lacunar stroke: pooled analysis of randomized trials. Stroke 2015; 46:1014.
22. SPS3 Investigators, Benavente OR, Hart RG, et al. Effects of clopidogrel added to aspirin in patients with recent lacunar stroke. N Engl J Med 2012; 367:817.
Leave a Reply