Hội chứng Guillain – Barre ở trẻ em là bệnh lý hiếm gặp, là nguyên nhân gây liệt mềm cấp. Nếu không được phát hiện và điều trị kịp thời, bệnh nhân Guillain – Barre có nguy cơ tử vong cao do suy hô hấp hoặc sặc phổi do rối loạn chức năng nuốt, hoặc ngừng tim do tổn thương thần kinh chi phối tim. Hội chứng Guillain – Barre là một bệnh lý thần kinh ngoại biên mắc phải được gọi là bệnh viêm đa rễ dây thần kinh mất myelin cấp tính (Acute Demyelinating Polyradiculoneuropathy) hoặc liệt Landry. Đây là chứng rối loạn do hệ miễn dịch tấn công vào một phần hệ thần kinh ngoại biên. Tình trạng này gây tổn thương dây thần kinh, gây viêm, dẫn đến liệt hoặc yếu cơ nếu không được chữa trị kịp thời.
Bài viết Hội chứng Guillain – Barré ở trẻ em trích nguồn từ Hội Thần kinh học Việt Nam.
Tác giả:
Đặng Hoàng Hưng1, Nguyễn Lê Trung Hiếu 1,2
Bộ môn Thần kinh, Đại học Y Dược TP. Hồ Chí Minh1
Khoa Thần kinh, Bệnh viện Nhi Đồng 22
Tóm tắt
Hội chứng Guillain – Barré là nguyên nhân thường gặp gây liệt mềm cấp tính, đặc trưng bởi yếu chi đối xứng kèm giảm hoặc mất phản xạ gân cơ, đạt mức độ nặng tối đa trong vòng 4 tuần.
Chẩn đoán hội chứng Guillain – Barré ở trẻ em là một thách thức vì nhiều lý do như giới hạn trong giao tiếp, thăm khám và sự đa dạng trong biểu hiện[11]. Chỉ khoảng một phần ba trẻ trước tuổi đến trường được chẩn đoán xác định hội chứng Guillain – Barré tại thời điểm nhập viện [26]. Việc đo điện cơ ở trẻ em cũng khó hơn so với người lớn. Kích thích gây đau làm nặng thêm tình trạng đau thần kinh sẵn có của trẻ, vì vậy không phải lúc nào cũng có thể đo đầy đủ các dây thần kinh và thực hiện điện cơ kim, và gần như không thể đo lặp lại [16].
Điều trị hội chứng Guillain – Barré ở trẻ em cho đến nay chưa có bằng chứng mạnh và vẫn sử dụng theo phác đồ tương tự của người lớn. Hội chứng Guillain – Barré ở trẻ em nhìn chung có tiên lượng tốt, nhưng đã có báo cáo tử vong do rối loạn chức năng thần kinh tự động hay do điều trị [28]. Nhiều yếu tố tiên lượng đã được nghiên cứu ở người lớn, tuy nhiên không nhiều trong số đó có thể áp dụng được ở trẻ em.
Từ khóa: Hội chứng Guilain Barré ở trẻ em.
1. Tổng quan
Hội chứng Guillain – Barré là nguyên nhân thường gặp nhất gây liệt mềm cấp tính, thường xảy ra sau nhiễm trùng, gây đáp ứng miễn dịch tạo nên các kháng thể làm tổn thương dây thần kinh hoặc gián đoạn chức năng dẫn truyền của dây thần kinh [29].
Hội chứng Guillain – Barré ở trẻ em có cùng đặc điểm chung là khởi đầu là tình trạng yếu chi đối xứng, tiến triển nhanh, đạt đỉnh triệu chứng trong vòng 4 tuần đầu, sau đó là giai đoạn bình nguyên kéo dài 2 ngày đến 6 tháng, trước khi bước vào giai đoạn hồi phục [8].
Tỷ lệ mắc mới hàng năm của Hội chứng Guillain – Barré ở trẻ em khá dao động tùy theo nghiên cứu, từ 0,4 – 1,4 ca trong 100.000 trẻ dưới 18 tuổi, thấp hơn so với người lớn [20]. Hiếm khi chúng ta thấy hội chứng Guillain – Barré ở trẻ dưới 2 tuổi. Tỷ lệ trẻ nam/trẻ nữ = 1,5/1.
76% bệnh nhân hội chứng Guillain – Barré nói chung có liên quan đến một sự kiện trong 4 tuần trước khi khởi bệnh, chủ yếu là nhiễm trùng đường hô hấp trên (36%) và viêm dạ dày ruột (27%) [7]. Chính sự liên quan mật thiết với nhiễm trùng nên có sự khác biệt tỷ lệ mới mắc giữa các mùa trong năm. Nhiều nghiên cứu ở các nước phương Tây gợi ý rằng đỉnh bệnh thường gặp vào mùa đông, trong khi ở một số nước châu Á thì lại đạt đỉnh vào các tháng mùa hè.
Cũng như ở người lớn, các báo cáo đã cho thấy mối liên quan giữa nhiễm trùng Campylobacter jejuni và Hội chứng Guillain – Barré thể AMAN[28]. Trong đại dịch COVID – 19, đã có các báo cáo về Hội chứng Guillain – Barré và hội chứng Miller Fisher liên quan với nhiễm virus SARS-CoV-2, mặc dù mối quan hệ nhân quả chưa được chứng minh [12].
2. Cơ chế bệnh sinh
Từ thời điểm được mô tả lần đầu, 1916 đến cuối những năm 1980, hội chứng Guillain – Barré được xem là bệnh lý thực thể đơn thuần do tình trạng tổn thương phức hợp myelin nguyên phát qua trung gian miễn dịch và tổn thương sợi trục thứ phát. Sau đó hội chứng Guillain – Barré được nghiên cứu rõ hơn và được chia làm hai thể: AIDP (Acute Inlfammatory Demyelinating Polyradiculoneuropathy) và AMAN (Acute Motor Axonal Neuropathy), dựa vào vị trí của kháng nguyên tổn thương thần kinh.
Các nghiên cứu tử thiết cho thấy AIDP đặc trưng bởi sự hiện diện của thâm nhiễm viêm của tế bào T và đại thực bào bao gồm các đại thực bào tạo myelin [2] (Hình 1.1A). Ngược lại với AIDP, bệnh nhân thể AMAN có tình trạng tổn thương sợi trục nguyên phát mà không kèm theo thâm nhiễm tế bào T hay hủy myelin mà thay vào đó là đại thực bào, bổ thể hoạt hóa và IgG lắng đọng ở màng sợi trục [10]. Đại thực bào xâm lấn vào khoang quanh sợi trục, làm rộng nốt, theo sau bởi bong myelin cận nốt, dẫn đến làm chậm tốc độ dẫn truyền (Hình 1.1B).
Sự khác biệt cơ chế bệnh sinh giữa AMAN và AIDP dẫn đến sự khác nhau khi hồi phục về lâm sàng và điện sinh lý. Ở AIDP, sự hồi phục phụ thuộc vào tình trạng tái tạo myelin và mức độ của thoái hóa sợi trục thứ phát. Còn ở AMAN, sự hồi phục phụ thuộc vào mức độ tổn thương do lắng đọng kháng thể. Quá trình này khá phức tạp vì các kháng thể gắn vào mầm của sợi trục và ngăn chặn sự tái tạo sợi trục [18]. Một số bệnh nhân thể AMAN hồi phục nhanh khi tình trạng block dẫn truyền do trung gian kháng thể được giải quyết.
Hình 1.1. Bệnh sinh miễn dịch của hội chứng Guillain – Barré. Nguồn: Yuki và cộng sự, 2012 [34].
Ganglioside là glycolipid chứa acid sialic xuất hiện nhiều ở hệ thần kinh của động vật có vú, đặc biệt ở nốt Ranvier và đầu tận thần kinh vận động (Hình 1.2). Các thể của hội chứng Guillain – Barré liên quan với các kháng thể kháng ganglioside đặc hiệu gợi ý sự phân bố không đồng đều của các glycolipid đích ở các dây thần kinh khác nhau. Chẳng hạn như hội chứng Guillain – Barré thể AMAN thường có các kháng thể IgG kháng GM1, GD1a và GalNAc – GD1a, hội chứng Miller – Fisher có kháng thể kháng GQ1b, biểu hiện ở vùng cận nốt của các thần kinh vận nhãn [5].
Kháng nguyên đích trong AIDP cho đến nay vẫn chưa được biết. Nhiều nghiên cứu thực nghiệm về viêm thần kinh tự miễn cho thấy protein myelin như PMP22, P0 và P2 và protein ở nốt như neurofascin có thể là kháng nguyên đích. Tuy nhiên các tự kháng thể kháng protein myelin chưa được phát hiện và kháng thể kháng neurofascin hiếm gặp ở bệnh nhân AIDP [21].
Hình 1.2. Cấu trúc các kháng thể kháng ganglioside trong hội chứng Guillain – Barré. Nguồn: Yuki và cộng sự, 2012 [34].
Trong hội chứng Guillain – Barré thể AMAN liên quan với Campylobacter jejuni, nhiều bằng chứng cho thấy vai trò của sự tương đồng cấu trúc phân tử có liên quan đến cơ chế bệnh sinh [23]; bệnh nhân bị hội chứng Guillain – Barré thể AMAN liên quan C.jejuni cũng có kháng thể kháng GM1 và GD1a; cấu trúc tương tự được phát hiện giữa thành phần đường của lipo-oligosaccharide của Campylobacter jejuni liên quan AMAN và ganglioside của thần kinh ngoại biên [34].
Cơ chế bệnh sinh của Hội chứng Guillain – Barré ở trẻ em cũng được mô tả trong Hội chứng Guillain – Barré chung.
3. Biểu hiện lâm sàng
Biểu hiện lâm sàng điển hình của hội chứng Guillain – Barré là dị cảm đầu ngón chân và đầu ngón tay, sau đó xuất hiện yếu tứ chi dưới đối xứng tăng dần, hai chi dưới nặng hơn hai chi trên, và trong trường hợp nặng có thể ảnh hưởng đến cơ hô hấp. Khoảng 9,6% trẻ cần thông khí cơ học [3].
Các triệu chứng thường gặp nhất của trẻ lúc nhập viện theo thứ tự [24]:
– Yếu tứ chi (93%)
– Đau thần kinh (73%)
– Yếu hai chi dưới (82%)
– Tổn thương thần kinh sọ (53%)
38% trẻ bị rối loạn thần kinh thực vật với một trong số các biểu hiện: rối loạn nhịp tim, huyết áp, rối loạn cơ vòng (bí tiểu, táo bón, liệt ruột), rối loạn thân nhiệt, rối loạn tiết mồ hôi [4].
Một số hiếm trẻ sẽ có biểu hiện của hệ thần kinh trung ương bởi tình trạng viêm thân não Bickerstaff.
Hội chứng Guillain – Barré diễn tiến một pha, thường đạt mức độ nặng tối đa trong vòng 4 tuần. 80% bệnh nhân đạt đỉnh triệu chứng trong 2 tuần và 97% đạt đỉnh trong 4 tuần, một bộ phận nhỏ bệnh nhân đạt đỉnh triệu chứng trong 4-6 tuần sau khi khởi phát [8]. Sau đó là giai đoạn bình nguyên kéo dài từ 2 ngày đến 6 tháng (trung bình là 7 ngày) trước khi bắt đầu hồi phục [8].
Bảng 1. Các thể của hội chứng Guillain – Barré. (Nguồn : Sonja E. Leonhard và cộng sự, 2019 [19])
| Thể lâm sàng | Tần suất | Biểu hiện lâm sàng |
| Hội chứng Guillain – Barré vận động cảm giác điển hình | 30 – 85% | Yếu và triệu chứng cảm giác đối xứng tiến triển nhanh, kèm giảm hoặc mất phản xạ gân cơ, thường đạt đỉnh trong vòng 2 tuần |
| Vận động đơn thuần | 5 – 70% | Yếu không kèm với triệu chứng cảm giác |
| Liệt hai chi dưới | 5 – 10% | Yếu khu trú hai chi dưới |
| Hầu họng – cổ – cánh tay | <5% | Yếu cơ hầu họng, cổ và cánh tay không kèm yếu chi |
| Liệt mặt hai bên kèm dị cảm | <5% | Liệt mặt hai bên, dị cảm và giảm phản xạ gân cơ |
| Cảm giác đơn thuần | <1% | Bệnh thần kinh cảm giác cấp hoặc bán cấp không kèm yếu liệt |
| Hội chứng Miller Fisher | 5 – 25% | Liệt vận nhãn, thất điều và mất phản xạ gân cơ. Thể không hoàn toàn với thất điều đơn thuần (bệnh thần kinh thất điều cấp tính) có thể xảy ra. Khoảng 15% bệnh nhân chồng lấp với hội chứng Guillain – Barré vận động cảm giác điển hình |
| Viêm thân não Bickerstaff | <5% | Liệt vận nhãn, thất điều, mất phản xạ gân cơ, dấu tháp và suy giảm ý thức, thường chồng lấp với hội chứng Guillain – Barré vận động cảm giác |
4. Cận lâm sàng
Dịch não tủy
Cũng như ở người lớn, khi nghi ngờ hội chứng Guillain – Barré, bệnh nhân sẽ được chọc dịch não tủy, mục đích chính là để loại trừ các chẩn đoán khác hơn là để xác định hội chứng Guillain – Barré. Tăng protein dịch não tủy và tế bào dịch não tủy bình thường (được gọi là phân ly đạm tế bào) được xem là chỉ điểm của hội chứng Guillain – Barré. Tuy nhiên, người ta thường nhầm lẫn rằng phân ly đạm tế bào là tiêu chuẩn cần có để chẩn đoán xác định, chỉ khoảng 64% bệnh nhân có phân ly đạm tế bào [8]. 50% bệnh nhân hội chứng Guillain – Barré có tăng protein dịch não tủy trong 3 ngày đầu và 80% sau tuần đầu tiên [8].
Khi tế bào dịch não tủy > 50/μL cần xem xét lại chẩn đoán hội chứng Guillain – Barré, và chẩn đoán phân biệt với các nguyên nhân khác như ung thư di căn màng não tủy, u lympho, viêm rễ thần kinh do CMV, bệnh đa dây thần kinh do HIV và bại liệt [8],[30]. Nếu nồng độ protein dịch não tủy bình thường, không cần thiết phải lặp lại chọc dịch não tủy để chẩn đoán hội chứng Guillain – Barré. Ngoài ra, điều trị với IVIg liều cao có thể làm tăng cả nồng độ protein lẫn tế bào dịch não tủy, có thể do dịch thấm lẫn viêm màng não vô trùng, gây bối rối trong việc chẩn đoán nếu ta chọc dịch não tủy lặp lại.
Đo dẫn truyền thần kinh
Điện cơ là xét nghiệm nhạy và đặc hiệu nhất trong chẩn đoán hội chứng Guillain – Barré, đồng thời xác định dạng tổn thương là myelin hay sợi trục. Tuy nhiên, đo điện cơ ở trẻ em cũng khó hơn so với người lớn. Việc kích thích gây đau làm nặng thêm tình trạng đau thần kinh sẵn có của trẻ, vì vậy không phải lúc nào cũng có thể đo đầy đủ các dây thần kinh và thực hiện điện cơ kim, và gần như không thể đo lặp lại [16]. Khi trẻ không dung nạp đo điện cơ, các xét nghiệm hình ảnh học như MRI hay siêu âm có thể làm sai lệch chẩn đoán [28].
Thể hủy myelin
Một số đặc điểm trên điện cơ giai đoạn sớm của hội chứng Guillain – Barré thể AIDP là tiềm thời kéo dài hoặc mất phản xạ Hoffmann và sóng F [9],[32]. Quả thực vậy, về mặt bệnh học, AIDP thường khởi phát ở rễ thần kinh. Sau đó, điện cơ dẫn truyền thường quy sẽ có hình ảnh tiềm thời kéo dài cùng các bằng chứng của hủy myelin từng đoạn, đặc biệt là block dẫn truyền và phát tán theo thời gian. Khoảng 50% bệnh nhân ở tuần thứ hai và 85% bệnh nhân ở tuần thứ ba sẽ xuất hiện những thay đổi này.
Hầu hết bệnh nhân sẽ có bất thường dẫn truyền vận động trong vài tuần đầu, nhưng bất thường điện cơ dẫn truyền cảm giác lại ít hơn nhiều. Giai đoạn sớm, điện cơ dẫn truyền cảm giác sẽ có kết quả bình thường. Sau một đến hai tuần đầu tiên, điện cơ dẫn truyền cảm giác sẽ có hình ảnh bảo tồn thần kinh bì bắp chân (sural sparing, nghĩa là đáp ứng cảm giác dây thần kinh bì bắp chân bình thường trong khi ở dây thần kinh giữa và trụ giảm hoặc biến mất). Đặc điểm này rất ít gặp trong bệnh đa dây thần kinh thể sợi trục.
Thể sợi trục
Đặc trưng của điện cơ trong hội chứng Guillain – Barré thể AMAN là giảm hoặc mất CMAP (compound muscle action potentials) và không có các đặc điểm của hủy myelin. Đối với thể AMAN, SNAP và điện cơ dẫn truyền thần kinh cảm giác bình thường. Ngay như tên gọi, đối với thể AMSAN (Acute Motor Sensory Axonal Neuropathy), bất thường vận động và cảm giác trên điện cơ đồng thời xuất hiện.
Trong giai đoạn sớm của hội chứng Guillain – Barré rất khó phân biệt giữa hai thể AIDP và AMAN, AMSAN vì một số trường hợp AMAN, AMSAN có kéo dài tiềm thời trong giai đoạn sớm, sau đó nhanh chóng hồi phục, trong khi đối với thể AIDP, tình trạng này ngày càng nặng [17].
Tiêu chuẩn điện cơ trong chẩn đoán hội chứng Guillain – Barré đã được đề cập và chỉnh sửa nhiều lần, gần đây nhất là tiêu chuẩn được đề xuất của tác giả Rajabally và cộng sự năm 2014.
Bảng 2. Tiêu chuẩn phân loại trên điện cơ (Nguồn: Rajabally và cộng sự, 2014 [22])
| Bình thường (tất cả các dây thần kinh được đo đều cho kết quả dưới đây) |
| DML ≤ 100% giới hạn bình thường trênHiện diện sóng F với tiềm thời ≤ 100% giới hạn bình thường trên
MCV ≥ 100% giới hạn bình thường dưới dCMAP ≥ 100% giới hạn bình thường dưới pCMAP ≥ 100% GHBT dưới Tỷ lệ pCMAP/dCMAP > 0,7 (trừ thần kinh chày) |
| Hội chứng Guillain – Barré thể AIDP |
| Ít nhất một trong các tiêu chuẩn dưới đây xuất hiện từ hai dây thần kinh trở lên:
MCV < 70% giới hạn bình thường dưới DML > 150% giới hạn bình thường trên Tiềm thời sóng F > 120% giới hạn bình thường trên, hoặc > 150% giới hạn bình thường trên (nếu CMAP ngọn chi < 50% giới hạn bình thường dưới) |
| Hội chứng Guillain – Barré thể AIDP |
| Hoặc– Không xuất hiện sóng F ở hai dây thần kinh có dCMAP ≥ 20% giới hạn bình thường dưới, kèm một trong các tiêu chuẩn trên xuất hiện ở một dây thần kinh khác
Hoặc – Tỷ số pCMAP/dCMAP < 0,7 (trừ thần kinh chày) ở hai dây thần kinh kèm một trong các tiêu chuẩn trên xuất hiện ở một dây thần kinh khác |
| Hội chứng Guillain – Barré thể AMAN bao gồm thể không kích thích được |
| Không có dây thần kinh nào thỏa tiêu chuẩn hủy myelin (trừ trường hợp một dây thần kinh có dCMAP < 10% giới hạn bình thường dưới thì có thể cho phép có một đặc điểm hủy myelin), và ít nhất một trong các đặc điểm sau:dCMAP < 80% GHBT dưới ở hai dây thần kinh
Không xuất hiện sóng F ở 2 dây thần kinh có dCMAP ≥ 20% giới hạn bình thường dưới và không kèm bất kỳ tiêu chuẩn hủy myelin ở bất kỳ dây thần kinh nào Tỷ số pCMAP/dCMAP < 0,7 ở hai dây thần kinh (trừ dây thần kinh chày) Không xuất hiện sóng F ở một dây thần kinh có dCMAP ≥ 20% giới hạn bình thường dưới HOẶC tỷ số pCMAP/dCMAP < 0,7 (trừ dây thần kinh chày) ở một dây thần kinh; kèm dCMAP < 80% giới hạn bình thường dưới ở một dây thần kinh khác. Không kích thích được: – dCMAP ngọn chi không xuất hiện ở tất cả dây thần kinh (hoặc xuất hiện chỉ ở một dây thần kinh với dCMAP ngọn chi < 10% giới hạn bình thường dưới) |
| Hội chứng Guillain – Barré thể AMSAN |
| Thỏa tiêu chuẩn điện cơ hội chứng Guillain – Barré thể AMAN kèm với:– SNAP ≤ 50% giới hạn bình thường dưới ở hai dây thần kinh |
| Không rõ |
| – Không phù hợp với bất kỳ tiêu chuẩn nào trong các nhóm trên |
| Chữ viết tắt: dCMAP: distal Compound Muscle Action Potentials, DML: Distal Motor Latency, MCV: Motor conduction Velocity, SNAP: Sensory Never Action Potentials. |
Điện cơ kim:
Việc khảo sát điện cơ kim ở trẻ em rất hạn chế, do đau. Trong Hội chứng Guillain – Barré việc khảo sát thường ở một, hai hoặc ba cơ, chẳng hạn cơ chày trước, cơ bụng chân trong, cơ gian cốt một mu tay, nhằm tìm kiếm hiện tượng mất phân bố thần kinh để đánh giá có hay không tổn thương sợi trục thứ phát.
5. Chẩn đoán
Chẩn đoán hội chứng Guillain – Barré ở trẻ em là một thách thức vì nhiều lý do như giới hạn trong giao tiếp, thăm khám và sự đa dạng trong biểu hiện [11]. Trong giai đoạn đầu, việc chẩn đoán chủ yếu dựa vào triệu chứng lâm sàng, khi mà các bất thường trên điện cơ hay dịch não tủy thường chưa xuất hiện, chẳng hạn ở trẻ em, biểu hiện đau chiếm ưu thế có thể che dấu tình trạng yếu chi và làm trì hoãn chẩn đoán [26]. Chỉ khoảng một phần ba trẻ trước tuổi đến trường được chẩn đoán xác định hội chứng Guillain – Barré tại thời điểm nhập viện [26].
Năm 1978, NINDS đã cho ra đời tiêu chuẩn chẩn đoán hội chứng Guillain – Barré đầu tiên khi đang nghiên cứu mối liên quan giữa hội chứng Guillain – Barré và chiến dịch chủng ngừa cúm lợn năm 1976 – 1977. Sau đó tiêu chuẩn này đã chính thức công bố năm 1981 và điều chỉnh bởi tác giả Asbury năm 1990 [1]. Ban đầu tiêu chuẩn được sử dụng trong nghiên cứu, sau đó được sử dụng rộng rãi trên lâm sàng cho đến nay. Tiêu chuẩn này được nghiên cứu trên người lớn và sau đó cũng được áp dụng rộng rãi ở trẻ em.
Cần lưu ý tiêu chuẩn này không áp dụng cho một số biến thể đặc biệt có trong Bảng 1.
Bảng 3. Tiêu chuẩn chẩn đoán hội chứng Guillain – Barré
Nguồn: Asbury và cộng sự [1]
| Đặc điểm cần cho chẩn đoán |
| Yếu 2 chân và 2 tay tăng dần (có thể khởi phát chỉ ở chân trong giai đoạn đầu)Giảm hoặc mất phản xạ gân cơ ở chi biểu hiện (tại vài thời điểm trong diễn tiến bệnh) |
| Đặc điểm hỗ trợ mạnh chẩn đoán |
| Pha diễn tiến từ vài ngày đến 4 tuần (thường < 2 tuần)Tương đối đối xứng về biểu hiện lâm sàng và thăm khám
Triệu chứng cảm giác tương đối nhẹ Tổn thương các dây thần kinh sọ, đặc biệt liệt thần kinh mặt hai bên Rối loạn thần kinh thực vật Đau chi hoặc đau cơ hoặc đau lưng lan kiểu rễ Tăng protein trong dịch não tủy; protein dịch não tủy bình thường không loại trừ chẩn đoán Đặc điểm của bệnh thần kinh vận động hoặc vận động cảm giác trên điện cơ (điện cơ bình thường trong giai đoạn sớm không loại trừ chẩn đoán) |
| Đặc điểm làm nghi ngờ chẩn đoán |
| Tăng số lượng bạch cầu đơn nhân và đa nhân trong dịch não tủy (> 50/mm3)Yếu chi không đối xứng rõ, kéo dài
Rối loạn cơ vòng bàng quang, ruột tại thời điểm khởi phát và kéo dài trong suốt quá trình bệnh Yếu cơ hô hấp nặng kèm yếu chi nhẹ tại thời điểm khởi phát Triệu chứng cảm giác kèm yếu chi nhẹ tại thời điểm khởi phát Sốt tại thời điểm khởi phát Đạt đỉnh trong < 24h Khoanh cảm giác rõ gợi ý tổn thương tủy sống Tăng phản xạ gân cơ hoặc clonus Phản xạ da lòng bàn chân đáp ứng duỗi Đau bụng Diễn tiến chậm kèm yếu chi nhẹ và không ảnh hưởng cơ hô hấp Tiếp tục diễn tiến > 4 tuần kể từ khi xuất hiện triệu chứng Thay đổi ý thức (trừ viêm thân não Bickerstaff) |
6. Điều trị
Điều trị hội chứng Guillain – Barré cần phải phối hợp đa mô thức và liệu pháp miễn dịch.
Liệu pháp miễn dịch
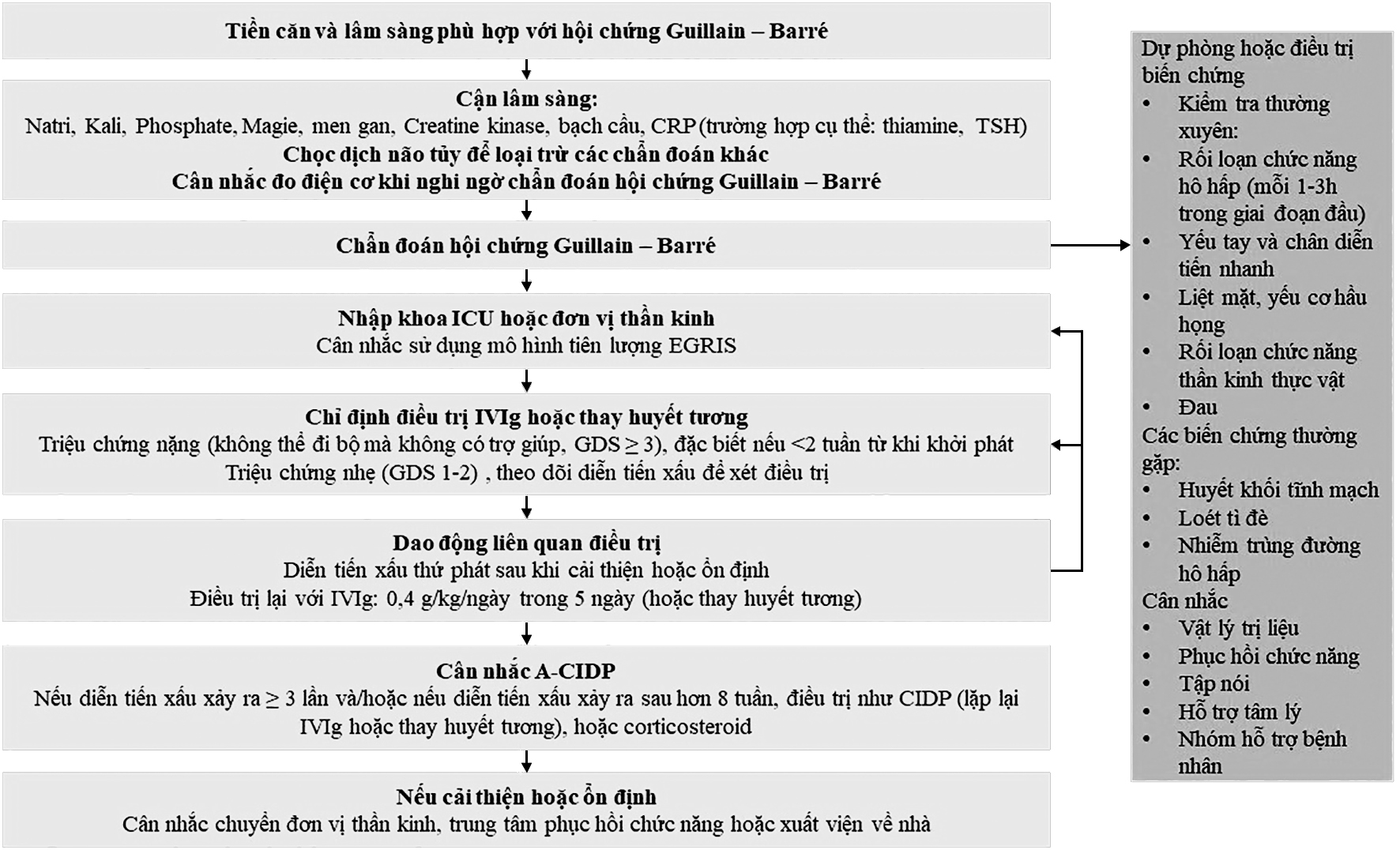
Trong điều trị pha cấp, IVIg và thay huyết tương đã được chứng minh có hiệu quả. Liệu pháp ức chế miễn dịch thường được khởi động khi bệnh nhân không thể đi được 10m mà không cần hồ trợ (GDS ≥ 3) (Hình 1.3). Khác với người lớn, bằng chứng về hiệu quả của các liệu pháp miễn dịch ở trẻ em còn hạn chế. Cho đến nay vẫn chưa có thử nghiệm lâm sàng ngẫu nhiên có đối chứng nào được thực hiện.
Hình 1.3. Chẩn đoán và điều trị hội chứng Guillain – Barré. Nguồn: Van den Berg và cộng sự, 2014 [43].
Bảng 4. Thang điểm GDS (GBS Disability Score). Nguồn: Hughes và cộng sự, 1978 [15]
| Điểm | Mô tả |
| 0 | Khỏe mạnh |
| 1 | Triệu chứng nhẹ và có thể chạy |
| 2 | Có thể đi ≥ 10 m và không cần trợ giúp nhưng không chạy được |
| 3 | Có thể đi 10 m trong không gian mở và cần sự trợ giúp |
| 4 | Nằm liệt giường hoặc ghế |
| 5 | Cần hỗ trợ thông khí trong ngày |
| 6 | Tử vong |
Nhiều thử nghiệm đã cho thấy không có sự khác biệt trong hiệu quả điều trị của IVIg và thay huyết tương [13].
Lựa chọn điều trị dựa trên bệnh nhân và các yếu tố kinh tế, xã hội. Ví dụ, thay huyết tương cần các thiết bị đặc biệt và không phải bệnh viện nào cũng có. Ngoài ra, thay huyết tương khó tiến hành ở trẻ nhỏ và cần phải theo dõi sát ở các bệnh nhân có rối loạn thần kinh thực vật tim mạch. Tuy nhiên, IVIg tốn chi phí cao hơn nhiều so với thay huyết tương, gây khó khăn trong tiếp cận điều trị, đặc biệt ở các nước thu nhập thấp.
Cho đến nay, liệu có sự khác biệt trong điều trị hội chứng Guillain – Barré thể tổn thương sợi trục và hủy myelin vẫn còn chưa rõ ràng. Một nghiên cứu đã cho thấy ở hội chứng Guillain – Barré thể tổn thương sợi trục, thay huyết tương có kết cục điều trị tốt hơn so với IVIg [6].
Đáp ứng điều trị
Khoảng 40 – 50% bệnh nhân sẽ không cải thiện với liệu pháp miễn dịch tại thời điểm 4 tuần sau điều trị [31].
Phối hợp điều trị thay huyết tương và theo sau bằng IVIg không mang lại hiệu quả cao hơn so với IVIg hay thay huyết tương một mình [14]. Việc lặp lại liều IVIg thứ 2 trong 4 tuần đầu khi chưa thấy đáp ứng với liều IVIg đầu tiên cũng không mang lại hiệu quả trong tiên lượng ngắn và dài hạn [31]. Kể cả những trường hợp có tiên lượng nặng thì việc lặp lại liều IVIg thứ 2 không giúp cải thiện tiên lượng, thậm chí còn có nhiều tác dụng phụ do điều trị gây ra [33].
Dao động liên quan điều trị (TRF – Treatment – Related Fluctuation) là tình trạng xấu đi sau khi đã cải thiện hoặc ổn định về mặt lâm sàng. TRF được định nghĩa là GDS tăng ít nhất 1 điểm trong vòng 8 tuần đầu sau khởi phát. Khoảng 8% trẻ có TRF [24] và tình trạng này thường gặp hơn khi sử dụng IVIg liều 1 g/kg/ngày 2 ngày so với liều 0,4 g/kg/ngày trong 5 ngày liên tiếp, dù về hiệu quả điều trị là tương đương nhau [16].
TRF cho thấy hiệu quả của điều trị, mặc dù không kéo dài, và sẽ lại cải thiện nếu chúng ta lặp lại điều trị. Hiện tại bằng chứng hiệu quả liều thứ 2 IVIg là chưa rõ ràng nhưng vẫn được áp dụng trên lâm sàng.
Khi tình trạng TRF xảy ra sau 8 tuần hoặc xảy ra ≥ 3 lần thì cần xem xét chẩn đoán A-CIDP.
7. Tiên lượng
Nhìn chung tiên lượng của hội chứng Guillain – Barré ở trẻ em tốt hơn so với người lớn. Tỷ lệ tử vong ở trẻ em vào khoảng 1 – 2% và chủ yếu là do suy hô hấp [27]. 11% trẻ bị tàn phế sau này và 26% trẻ bị ảnh hưởng tới việc học tập, trẻ càng lớn thì việc học càng bị ảnh hưởng nhiều [25].
8. Kết luận
Hội chứng Guillain – Barré là nguyên nhân thường gặp nhất gây liệt mềm cấp ở trẻ em. Diễn tiến bệnh thường là 1 pha, đạt đỉnh trong vòng 4 tuần. Việc chẩn đoán và điều trị ở trẻ em gặp nhiều thách thức hơn so với người lớn vì giới hạn trong giao tiếp, thăm khám, sự đa dạng trong biểu hiện và khó khăn trong đo điện cơ. Còn nhiều khoảng trống trong điều trị, đặc biệt ở nhóm đáp ứng kém và dao động với IVIg và thay huyết tương. Tiên lượng hội chứng Guillain – Barré ở trẻ em nhìn chung là tốt hơn so với người lớn, tuy nhiên vẫn có một nhóm trẻ bị ảnh hưởng đến việc học và để lại di chứng lâu dài về sau này.
Phụ lục: Trị số bình thường của đo điện cơ dẫn truyền ở trẻ em [35]
Người dịch: Lê Trần Ánh Ngân2, Nguyễn Lê Trung Hiếu1.2
| Tuổi | Tiềm thời ngọn chi (ms) | Biên độ (mV) | Vận tốc dẫn truyền (m/s) |
| Thần kinh giữa | |||
| 23-29 tuần | Bất kỳ | ≥ 7 | |
| 29-33 tuần | Bất kỳ | ≥ 16 | |
| 33-38 tuần | ≤ 3,8 | Bất kỳ | ≥ 19 |
| Đủ tháng (38-42 tuần) | ≤ 3,5 | ≥ 2,5 | ≥ 20 |
| 2-4 tuần | ≤ 3,0 | ≥ 2,5 | ≥ 23 |
| 1-6 tháng | ≤ 3,0 | ≥ 3,5 | ≥ 30 |
| 6-12 tháng | ≤ 3,0 | ≥ 2,3 | ≥ 35 |
| 12-18 tháng | ≤ 3,0 | ≥ 3,7 | ≥ 40 |
| 18-24 tháng | ≤ 3,0 | ≥ 3,7 | ≥ 45 |
| 2-3 tuổi | ≤ 3,1 | ≥ 2,0 | ≥ 47 |
| 3-4 tuổi | ≤ 3,1 | ≥ 2,0 | ≥ 48 |
| 4-5 tuổi | ≤ 3,2 | ≥ 3,0 | ≥ 49 |
| Người lớn | ≤ 4,5 | ≥ 4,1 | ≥ 49 |
| Thần kinh trụ | |||
| 34-37 tuần | ≤ 3,0 | – | ≥ 15 |
| Đủ tháng | ≤ 3,5 | ≥ 1,0 | ≥ 20 |
| 0-1 tháng | ≤ 3,5 | ≥ 2,0 | ≥ 20 |
| 1-6 tháng | ≤ 3,0 | ≥ 2,5 | ≥ 30 |
| 6-12 tháng | ≤ 2,5 | ≥ 3,0 | ≥ 35 |
| 1-2 tuổi | ≤ 2,5 | ≥ 3,0 | ≥ 40 |
| 2-3 tuổi | ≤ 2,5 | ≥ 3,0 | ≥ 45 |
| 3-4 tuổi | ≤ 2,5 | ≥ 3,0 | ≥ 50 |
| 4-5 tuổi | ≤ 2,7 | ≥ 3,0 | ≥ 50 |
| Người lớn | ≤ 3,7 | ≥ 6,0 | ≥ 50 |
| Thần kinh mác | |||
| Đủ tháng | ≤ 4,5 | ≥ 0,5 | ≥ 20 |
| Tháng | ≤ 4,5 | ≥ 0,5 | ≥ 20 |
| 1-6 tháng | ≤ 3,2 | ≥ 0,5 | ≥ 27 |
| 6-12 tháng | ≤ 3,2 | ≥ 0,7 | ≥ 36 |
| 1-2 tuổi | ≤ 3,2 | ≥ 0,7 | ≥ 38 |
| 2-3 tuổi | ≤ 4,1 | ≥ 0,9 | ≥ 39 |
| 3-4 tuổi | ≤ 4,1 | ≥ 1,0 | ≥ 40 |
| 4-6 tuổi | ≤ 4,1 | ≥ 1,3 | ≥ 40 |
| Người lớn | ≤ 6,5 | ≥ 2,0 | ≥ 40 |
| Thần kinh chày | |||
| 23-29 tuần | – | – | ≥ 6 |
| 29-33 tuần | – | – | ≥ 9 |
| 33-38 tuần | ≤ 4,7 | – | ≥ 13 |
| Đủ tháng (38-42 tuần) | ≤ 4,1 | ≥ 0,9 | ≥ 17 |
| 1-3 tháng | ≤ 4,0 | ≥ 1,2 | ≥ 20 |
| 3-6 tháng | ≤ 3,5 | ≥ 1,2 | ≥ 25 |
| 6-9 tháng | ≤ 3,5 | ≥ 3,4 | ≥ 30 |
| 9-12 tháng | ≤ 3,5 | ≥ 3,4 | ≥ 32 |
| 1-3 tuổi | ≤ 4,0 | ≥ 4,8 | ≥ 33 |
| 3-6 tuổi | ≤ 4,7 | ≥ 4,8 | ≥ 40 |
| Người lớn | ≤ 6,1 | ≥ 4,4 | ≥ 40 |
| Tuổi | Biên độ (μV) | Vận tốc dẫn truyền (m/s) |
| Thần kinh giữa | ||
| Đủ tháng | ≥ 3,5 | ≥ 22 |
| 0-1 tháng | ≥ 3,5 | ≥ 24 |
| 1-3 tháng | ≥ 5 | ≥ 25 |
| 3-6 tháng | ≥ 5 | ≥ 32 |
| 6-12 tháng | ≥ 5 | ≥ 33 |
| 1-2 tuổi | ≥ 9 | ≥ 41 |
| 2-4 tuổi | ≥ 13 | ≥ 45 |
| 4-6 tuổi | ≥ 14 | ≥ 48 |
| Thần kinh trụ | ||
| 34-36 tuần | – | ≥ 10 |
| Đủ tháng | ≥ 4 | ≥ 13 |
| 2-4 tuần | ≥ 6 | ≥ 17 |
| 1-3 tháng | ≥ 6 | ≥ 20 |
| 3-6 tháng | ≥ 6 | ≥ 26 |
| 6-12 tháng | ≥ 6 | ≥ 28 |
| 1-3 tuổi | ≥ 6 | ≥ 29 |
| 4-6 tuổi | ≥ 6 | ≥ 33 |
| Thần kinh sural | ||
| Đủ tháng | Bất kì | ≥ 18 |
| 0-1 tháng | Bất kì | ≥ 21 |
| 1-3 tháng | Bất kì | ≥ 23 |
| 3-6 tháng | Bất kì | ≥ 26 |
| 6-12 tháng | Bất kì | ≥ 30 |
| 1-2 tuổi | ≥ 6 | ≥ 34 |
| 2-4 tuổi | ≥ 6 | ≥ 38 |
| 4-6 tuổi | ≥ 6 | ≥ 41 |
| Thần kinh gan bàn chân trong | ||
| Đủ tháng | ≥ 10 | – |
| 1-6 tháng | ≥ 15 | ≥ 35 |
| 6-12 tháng | ≥ 15 | ≥ 40 |
| 1-2 tuổi | ≥ 15 | ≥ 40 |
Tài liệu tham khảo
1. Asbury A. K., Cornblath D. R. (1990), “Assessment of current diagnostic criteria for Guillain-Barré syndrome”. Ann Neurol, 27 Suppl, pp. Number of S21-4.
2. Asbury A. K., Arnason B. G., Adams R. D. (1969), “The inflammatory lesion in idiopathic polyneuritis. Its role in pathogenesis”. Medicine (Baltimore), 48 (3), pp. Number of 173-215.
3. Barzegar M., Toopchizadeh V., Golalizadeh D., Pirani A., Jahanjoo F. (2020), “A Predictive Model for Respiratory Failure and Determining the Risk Factors of Prolonged Mechanical Ventilation in Children with Guillain-Barre Syndrome”. Iran J Child Neurol, 14 (3), pp. Number of 33-46.
4. Chakraborty T., Kramer C. L., Wijdicks E. F. M., Rabinstein A. A. (2020), “Dysautonomia in Guillain-Barré Syndrome: Prevalence, Clinical Spectrum, and Outcomes”. Neurocrit Care, 32 (1), pp. Number of 113-120.
5. Chiba A., Kusunoki S., Obata H., Machinami R., Kanazawa I. (1993), “Serum anti-GQ1b IgG antibody is associated with ophthalmoplegia in Miller Fisher syndrome and Guillain-Barré syndrome: clinical and immunohistochemical studies”. Neurology, 43 (10), pp. Number of 1911-7.
6. Dada M. A., Kaplan A. A. (2004), “Plasmapheresis treatment in Guillain-Barré syndrome: potential benefit over IVIg in patients with axonal involvement”. Ther Apher Dial, 8 (5), pp. Number of 409-12.
7. Doets A. Y., Verboon C., van den Berg B., Harbo T., Cornblath D. R., et al. (2018), “Regional variation of Guillain-Barré syndrome”. Brain, 141 (10), pp. Number of 2866-2877.
8. Fokke C., van den Berg B., Drenthen J., Walgaard C., van Doorn P. A., et al. (2014), “Diagnosis of Guillain-Barré syndrome and validation of Brighton criteria”. Brain, 137 (Pt 1), pp. Number of 33-43.
9. Gordon P. H., Wilbourn A. J. (2001), “Early electrodiagnostic findings in Guillain-Barré syndrome”. Arch Neurol, 58 (6), pp. Number of 913-7.
10. Hafer-Macko C., Hsieh S. T., Li C. Y., Ho T. W., Sheikh K., et al. (1996), “Acute motor axonal neuropathy: an antibody-mediated attack on axolemma”. Ann Neurol, 40 (4), pp. Number of 635-44.
11. Hasan I., Papri N., Hayat S., Jahan I., Ara G., et al. (2021), “Clinical and serological prognostic factors in childhood Guillain-Barré syndrome: A prospective cohort study in Bangladesh”. J Peripher Nerv Syst, 26 (1), pp. Number of 83-89.
12. Hasan I., Saif-Ur-Rahman K. M., Hayat S., Papri N., Jahan I., et al. (2020), “Guillain-Barré syndrome associated with SARS-CoV-2 infection: A systematic review and individual participant data meta-analysis”. J Peripher Nerv Syst, 25 (4), pp. Number of 335-343.
13. Hughes R. A., Swan A. V., van Doorn P. A. (2014), “Intravenous immunoglobulin for Guillain-Barré syndrome”. Cochrane Database Syst Rev, 2014 (9), pp. Number of Cd002063.
14. Hughes R. A., Swan A. V., Raphaël J. C., Annane D., van Koningsveld R., et al. (2007), “Immunotherapy for Guillain-Barré syndrome: a systematic review”. Brain, 130 (Pt 9), pp. Number of 2245-57.
15. Hughes R. A., Newsom-Davis J. M., Perkin G. D., Pierce J. M. (1978), “Controlled trial prednisolone in acute polyneuropathy”. Lancet, 2 (8093), pp. Number of 750-3.
16. Korinthenberg R., Schessl J., Kirschner J. (2007), “Clinical presentation and course of childhood Guillain-Barré syndrome: a prospective multicentre study”. Neuropediatrics, 38 (1), pp. Number of 10-7.
17. Kuwabara S., Ogawara K., Misawa S., Koga M., Mori M., et al. (2004), “Does Campylobacter jejuni infection elicit “demyelinating” Guillain-Barre syndrome?”. Neurology, 63 (3), pp. Number of 529-33.
18. Lehmann H. C., Lopez P. H., Zhang G., Ngyuen T., Zhang J., et al. (2007), “Passive immunization with anti-ganglioside antibodies directly inhibits axon regeneration in an animal model”. J Neurosci, 27 (1), pp. Number of 27-34.
19. Leonhard S. E., Mandarakas M. R., Gondim F. A. A., Bateman K., Ferreira M. L. B., et al. (2019), “Diagnosis and management of Guillain-Barré syndrome in ten steps”. Nat Rev Neurol, 15 (11), pp. Number of 671-683.
20. McGrogan A., Madle G. C., Seaman H. E., de Vries C. S. (2009), “The epidemiology of Guillain-Barré syndrome worldwide. A systematic literature review”. Neuroepidemiology, 32 (2), pp. Number of 150-63.
21. Ng J. K., Malotka J., Kawakami N., Derfuss T., Khademi M., et al. (2012), “Neurofascin as a target for autoantibodies in peripheral neuropathies”. Neurology, 79 (23), pp. Number of 2241-8.
22. Rajabally Y. A., Durand M. C., Mitchell J., Orlikowski D., Nicolas G. (2015), “Electrophysiological diagnosis of Guillain-Barré syndrome subtype: could a single study suffice?”. J Neurol Neurosurg Psychiatry, 86 (1), pp. Number of 115-9.
23. Rees J. H., Soudain S. E., Gregson N. A., Hughes R. A. (1995), “Campylobacter jejuni infection and Guillain-Barré syndrome”. N Engl J Med, 333 (21), pp. Number of 1374-9.
24. Roodbol J., de Wit M. Y., van den Berg B., Kahlmann V., Drenthen J., et al. (2017), “Diagnosis of Guillain-Barré syndrome in children and validation of the Brighton criteria”. J Neurol, 264 (5), pp. Number of 856-861.
25. Roodbol J., de Wit M. C., Aarsen F. K., Catsman-Berrevoets C. E., Jacobs B. C. (2014), “Long-term outcome of Guillain-Barré syndrome in children”. J Peripher Nerv Syst, 19 (2), pp. Number of 121-6.
26. Roodbol J., de Wit M. C., Walgaard C., de Hoog M., Catsman-Berrevoets C. E., et al. (2011), “Recognizing Guillain-Barre syndrome in preschool children”. Neurology, 76 (9), pp. Number of 807-10.
27. Ryan M. M. (2005), “Guillain-Barré syndrome in childhood”. J Paediatr Child Health, 41 (5-6), pp. Number of 237-41.
28. Shahrizaila N., Lehmann H. C., Kuwabara S. (2021), “Guillain-Barré syndrome”. Lancet, 397 (10280), pp. Number of 1214-1228.
29. van den Berg B., Walgaard C., Drenthen J., Fokke C., Jacobs B. C., et al. (2014), “Guillain-Barré syndrome: pathogenesis, diagnosis, treatment and prognosis”. Nat Rev Neurol, 10 (8), pp. Number of 469-82.
30. van Doorn P. A., Ruts L., Jacobs B. C. (2008), “Clinical features, pathogenesis, and treatment of Guillain-Barré syndrome”. Lancet Neurol, 7 (10), pp. Number of 939-50.
31. Verboon C., van Doorn P. A., Jacobs B. C. (2017), “Treatment dilemmas in Guillain-Barré syndrome”. J Neurol Neurosurg Psychiatry, 88 (4), pp. Number of 346-352.
32. Vucic S., Cairns K. D., Black K. R., Chong P. S., Cros D. (2004), “Neurophysiologic findings in early acute inflammatory demyelinating polyradiculoneuropathy”. Clin Neurophysiol, 115 (10), pp. Number of 2329-35.
33. Walgaard C., Jacobs B. C., Lingsma H. F., Steyerberg E. W., van den Berg B., et al. (2021), “Second intravenous immunoglobulin dose in patients with Guillain-Barré syndrome with poor prognosis (SID-GBS): a double-blind, randomised, placebo-controlled trial”. Lancet Neurol, 20 (4), pp. Number of 275-283.
34. Yuki N., Hartung H. P. (2012), “Guillain-Barré syndrome”. N Engl J Med, 366 (24), pp. Number of 2294-304.
35. McMillan Hugh J., Kang Peter B. (2017), “Pediatric Electromyography: Concepts and Clinical Applications”, Springer, Canada, pp. 373-378.


Leave a Reply