Statin là thuốc điều trị rối loạn lipid máu được khuyến cáo đầu tay trong việc kiểm soát lipid máu và giảm các nguy cơ tim mạch. Đây là nhóm thuốc được chỉ định hàng đầu trong điều trị rối loạn lipid máu vì các bằng chứng từ các nghiên cứu lâm sàng cho thấy hiệu quả rất rõ ràng.
1.Lịch sử
- Thuốc ức chế HMG-CoA reductase, hay còn gọi với cái tên quen thuộc là statin, là một loại thuốc chính dùng để điều trị rối loạn lipid máu và dự phòng các biến cố tim mạch.
- Lý thuyết đầu tiên về việc cholesterol có liên quan đến vữa xơ động mạch bắt đầu từ đầu thế kỷ XX, tuy nhiên khi đó cholesterol chưa được chú ý nhiều. Đầu những năm 1950, John Gofman, đại học Berkeley – California đã thực hiện những nghiên cứu dịch tễ học và thấy rằng những cơn đau tim liên quan đến tăng LDL (lipoprotein tỷ trọng thấp), trong khi HDL (lipoprotein tỷ trọng cao) tăng, các cơn đau tim ít xảy ra hơn.
- HMG-CoA reductase là enzyme kiểm soát tốc độ tổng hợp cholesterol tại gan. Các nhà khoa học nhanh chóng nhận ra sự tương đồng về cấu trúc giữa compactin và HMG-CoA (cơ chất của enzyme). Do đó, cơ chế hoạt động compactin được đề xuất là ức chế cạnh tranh với enzyme.
Tháng 7/1982, Merck bắt đầu các thử nghiệm lâm sàng quy mô lớn về lovastatin trên những bệnh nhân có nguy cơ cao và nghiên cứu độc tính lâu dài trên chó năm 1984. Thuốc cho thấy tác dụng hạ cholesterol máu đáng kể và được dung nạp tốt, đồng thời không quan sát thấy khối u nào trên chó. Năm 1987, FDA đã cấp phép lưu hành lovastatin. Sau đó, có thêm 5 statin được thương mại hóa, bao gồm hai statin bán tổng hợp (simvastatin và pravastatin), 3 statin tổng hợp (Rosuvastatin, atorvastatin và pitavastatin).
2.Dược lý học
- Statin là thuốc điều trị rối loạn lipid máu được khuyến cáo đầu tay trong việc kiểm soát lipid máu và giảm các nguy cơ tim mạch. Đây là nhóm thuốc được chỉ định hàng đầu trong điều trị rối loạn lipid máu vì các bằng chứng từ các nghiên cứu lâm sàng cho thấy hiệu quả rất rõ ràng.
- Các statin mạnh vẫn là ưu tiên lựa chọn hàng đầu trong điều trị các rối loạn lipid máu, đặc biệt trên những bệnh nhân tăng lipid máu có tính chất gia đình, bệnh nhân nguy cơ tim mạch rất cao, nguy cơ cao, trung bình.
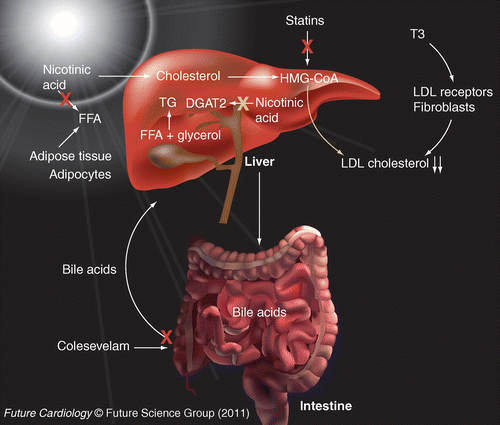
- Statin là chất ức chế cạnh tranh của enzyme khử 3-hydroxy-3-methylglutaryl coenzyme A (HMG-CoA) chịu trách nhiệm cho chuyển đổi HMG-CoA thành mevalonate, tiền chất của sterol, bao gồm cholesterol. Sự ức chế sinh tổng hợp cholesterol trong các tế bào gan kích thích hơn nữa sự tổng hợp các thụ thể LDL, do đó làm tăng sự hấp thu LDL, làm giảm LDL-C trong máu.
- Tất cả các statin được hấp thụ nhanh, tối đa trong vòng 4h. Tuy nhiên, thời gian bán hủy của các thuốc thay đổi đáng kể. Atorvastatin và rosuvastatin có thời gian bán hủy dài hơn nên hiệu quả giảm cholesterol kéo dài cả ngày.
- Tất cả các statin, ngoại trừ pravastatin, đều có tỷ lệ gắn protein huyết tương cao và các statin này có khả năng thay thế các thuốc liên kết với albumin, như warfarin. Ví dụ, dùng chung rosuvastatin hoặc simvastatin có thể dẫn đến tăng thời gian prothrombin
- Statin chuyển hóa tại gan thông qua các enzyme cytochrome P450 (CYP). Tương tác giữa statin và các thuốc khác xảy ra do sự tác động qua lại với các isoenzyme CYP do kích thích hoặc ức chế.
- Các thuốc nhóm này không nên dùng quá gần bữa ăn và có thể dùng 1 lần trong ngày trước khi đi ngủ. Các statin khác nhau có hiệu lực giảm nồng độ LDL-C khác nhau. Thực tế, liều dùng của statin được tính dựa trên hoạt lực và đích điều trị cần đạt (LDL-C).
3. Chỉ định
Statin được chỉ định chính trong điều trị rối loạn lipid máu để phòng ngừa các biến cố tim mạch tiên phát và thứ phát.
Mục tiêu điều trị dựa trên phân tầng nguy cơ và nồng độ các thành phần lipid máu. Tùy theo tầng nguy cơ mà có một đích điều trị khác nhau. Những thành phần lipid máu được khuyến cáo là chỉ số xác định đích điều trị như sau:
- LDL-C là đích điều trị chính.
- Cholesterol toàn phần (TC) có thể coi là đích điều trị nếu không có các xét nghiệm khác.
- Nên đánh giá trong quá trình điều trị để có kế hoạch can thiệp khi bệnh nhân rối loạn lipid máu có tăng triglyceride nhiều.
- Non-HDL-C hoặc Apo B là đích điều trị thứ hai ở bệnh nhân rối loạn lipid máu thể hỗn hợp, đái tháo đường, hội chứng chuyển hóa hoặc bệnh thận mạn.
- Tỷ lệ apoB/apoA1 và non-HDL-C/HDL-C không còn được khuyến cáo là đích điều trị thường quy.
3.1 Mục tiêu điều trị rối loạn lipid máu (theo ESC 2019): Dự phòng tiên phát:
- Nhóm nguy cơ rất cao: Mục tiêu giảm LDL-C ≥ 50% so với mức nền (khi bệnh nhân chưa được điều trị bằng bất kỳ thuốc hạ lipid máu nào) và đích LDL-C < 1,4 mmol/L (< 55 mg/dL).
- Nhóm nguy cơ cao: Mục tiêu giảm LDL-C ≥ 50% so với mức nền (khi bệnh nhân chưa được điều trị bằng bất kỳ thuốc hạ lipid máu nào) và đích LDL-C dưới 1,8 mmol/L (< 100 mg/dL).
- Nhóm nguy cơ vừa: Mức LDL-C tốt nhất dưới 2,6 mmol/L (< 115 mg/dL). Nhóm nguy cơ thấp: Mức LDL-C tốt nhất dưới 3,0 mmol/L (< 116 mg/dL). Mục tiêu phụ bao gồm: Non – HDL; apo-B. Trong đó mục tiêu của non-HDL tương ứng với mục tiêu LDL-C + 0,8 mmol/L cho từng nhóm nguy cơ nói trên. Mục tiêu của apo-B cho các nhóm bệnh nhân nguy cơ rất cao, cao và trung bình lần lượt là 65,80 và 100 mg/dL.
3.2 Dự phòng thứ phát:
- Nguy cơ rất cao: Mục tiêu giảm LDL-C ≥ 50% so với mức nền (khi bệnh nhân chưa được điều trị bằng bất kỳ thuốc hạ lipid máu nào) và đích LDL-C < 1,4 mmol/L (< 55 mg/dL).
- Nếu bệnh nhân đang điều trị liều statin tối đa dung nạp được xảy ra biến cố tim mạch lần 2 (không nhất thiết phải cùng một loại biến cố tim mạch lần đầu) trong vòng 2 năm, có thể cân nhắc thay đổi mục tiêu LDL-C thành 1,0 mmol/L.
4. Chống chỉ định
- Phụ nữ đang mang thai và cho con bú do ảnh hưởng tới thai nhi.
- Bệnh nhân mắc bệnh gan giai đoạn hoạt động hoặc tăng men gan kéo dài không giải thích được.
- Bệnh nhân quá mẫn cảm với bất kỳ thành phần nào của thuốc.
- Simvastatin và lovastatin bị chống chỉ định khi sử dụng đồng thời với các chất ức chế CYP3A4 mạnh (ví dụ: itraconazole, ketoconazole, posaconazole, voriconazole, ức chế HIV protease, boceprevir, telaprevir, kháng sinh macrolid erythromycin và clarithromycin, kháng sinh ketolid telithromycin, thuốc chống trầm cảm nefazodone sản phẩm chứa cobicistat). Simvastatin chống chỉ định ở những bệnh nhân sử dụng, cyclosporin hoặc danazol. Pitavastatin chống chỉ định trong khi dùng đồng thời cyclosporine.
5. Tác dụng không mong muốn
5.1 Tổn thương cơ
Là một tác dụng không mong muốn phổ biến khi sử dụng statin. Tổn thương cơ có thể ở dạng tiêu cơ vân có hoặc không có tổn thương thận cấp. Sử dụng statin với các chất ức chế CYP làm tăng nguy cơ tổn thương cơ và nên ngừng sử dụng nếu nồng độ CK tăng cao rõ rệt hoặc bệnh cơ được chẩn đoán hoặc nghi ngờ.
Chỉnh liều statin được khuyến cáo khi sử dụng cùng, cyclosporin hoặc thuốc ức chế CYP3A4. Cần thận trọng ở những bệnh nhân có yếu tố dễ gây tổn thương cơ: Trên 65 tuổi, nữ, suy giáp chưa được điều trị hoặc suy thận. Các triệu chứng tại cơ thường hết trong vòng 2 tháng sau khi ngừng thuốc.
Nếu các triệu chứng từ nhẹ đến trung bình, có thể tạm ngừng statin cho đến khi các triệu chứng được đánh giá lại. Nếu các triệu chứng đau cơ hết và nếu không còn chống chỉ định, bệnh nhân có thể được sử dụng liều ban đầu hoặc liều thấp hơn để tìm mối liên quan giữa các triệu chứng tại cơ và liệu pháp statin. Nếu đau cơ xuất hiện trở lại nên ngừng sử dụng statin cho đến khi các triệu chứng đau cơ hết, bắt đầu dùng liều lại và đổi sang statin khác.
Các thuốc điều trị rối loạn lipid khác (như ezetimibe, chất cô lập acid mật (BAS) và niacin) là thuốc thay thế ở bệnh nhân không dung nạp statin.
5.2 Tổn thương gan:
Với mức tăng alanine aminotransferase (ALT) nhỏ hơn 1,2% và tăng lên 2,3% với liều cao. Tăng men gan thường xảy ra trong 3 tháng đầu điều trị (có thể liên quan đến thay đổi thành phần lipid của màng tế bào gan, dẫn đến tăng tính thấm). Nên kiểm tra nồng độ AST và ALT trước khi bắt đầu điều trị. Tổn thương gan nặng do statin là rất hiếm. Tuy nhiên, nếu có tổn thương gan và không tìm thấy nguyên nhân khác, cần giảm liều hoặc đổi sang thuốc điều trị rối loạn lipid máu khác.
5.3 Giảm trí nhớ và nhầm lẫn
Cũng đã được báo cáo khi sử dụng statin; tuy nhiên, những triệu chứng này rất hiếm gặp, thường không nghiêm trọng, không dẫn đến suy giảm nhận thức và thường phục hồi sau khi ngừng sử dụng statin. Thời gian khởi phát rất thay đổi, từ một ngày đến nhiều năm sau khi sử dụng thuốc.
5.4 Tăng nguy cơ mắc bệnh đái tháo đường:
Điều trị bằng statin có liên quan đến tăng tỷ lệ đái tháo đường mới xuất hiện. Trong một phân tích tổng hợp trên 13 nghiên cứu trên 91.140 bệnh nhân, nhóm sử dụng statin tăng 9% nguy cơ đái tháo đường type 2 có ý nghĩa thống kê. Nguy cơ này cao hơn ở nhóm người cao tuổi.
Phân tích kết quả của nghiên cứu JUPITER cho thấy nguy cơ đái tháo đường cao hơn ở những nhóm bệnh nhân có một hoặc nhiều hơn các yếu tố nguy cơ đái tháo đường. Các bằng chứng khác cũng ủng hộ quan điểm này liên quan đến nhiều thuốc thuộc nhóm statin như rosuvastatin, atorvastatin, pravastatin. Cơ chế của hiện tượng này có thể liên quan đến tình trạng giảm tiết insulin ở tụy và giảm nhạy cảm của insulin ở ngoại biên.
Leave a Reply