Ung thư biểu mô tế bào gan (UTBMTBG) là loại tổn thương thường gặp nhất trong các loại ung thư tại gan, nằm trong sáu loại ung thư phổ biến nhất trên thế giới và nằm trong ba loại ung thư phổ biến nhất tại Việt Nam. UTBMTBG đứng đầu trong các nguyên nhân tử vong liên quan đến ung thư tại Việt Nam.
1. DỊCH TỄ HỌC UTBMTBG VÀ CÁC YẾU TỐ NGUY CƠ
1.1. Dịch tễ học
UTBMTBG là loại ung thư thường gặp nhất và là nguyên nhân hàng đầu gây tử vong liên quan đến ung thư tại Việt Nam theo ước tính của Tổ chức Ghi nhận Ung thư toàn cầu (GLOBOCAN) năm 2018. Tại Việt Nam chưa có số liệu quốc gia được công bố chính thức về xuất độ UTBMTBG. Một nghiên cứu ghi nhận số liệu UTBMTBG tại miền Trung và miền Nam Việt Nam là 24091 trường hợp trong thời gian 2010 đến 2016, trong đó 62,3% có nhiễm virus viêm gan B (HBV) mạn và 26% có nhiễm virus viêm gan C (HCV) mạn. Việt Nam là nước có xuất độ nhiễm HBV cao, ước tính có khoảng 12,3% nam giới và 8,8% nữ giới có nhiễm HBV mạn. Tuy việc chủng ngừa HBV cho trẻ em tại Việt Nam đã làm giảm phần nào xuất độ viêm gan virus B mạn, nhưng vẫn đang có tình trạng bùng phát ung thư biểu mô tế bào gan liên quan đến nhiễm HBV tại Việt Nam.
1.2. Các yếu tố nguy cơ chính
– HBV: theo số liệu của Tổ chức Y tế Thế giới (WHO) năm 2016, dựa trên một số nghiên cứu từ 2003 đến 2014, tỉ lệ nhiễm HBV ở người lớn tại Việt Nam khoảng 8,2-19%. Nhiều nghiên cứu phân tích gộp (meta-analysis) đã chứng tỏ nguy cơ UTBMTBG ở những người nhiễm HBV cao hơn 15-20 lần so với những người không nhiễm. Nguy cơ bị UTBMTBG trong cuộc đời của người nhiễm HBV mạn là khoảng 10-25%. Có nhiều yếu tố làm tăng nguy cơ UTBMTBG ở người nhiễm HBV mạn, bao gồm các yếu tố về hình thái (nam giới, tuổi lớn, tiền sử gia đình có người bị UTBMTBG), về virus (mức độ nhân bản HBV cao, kiểu hình HBV, thời gian nhiễm HBV, đồng nhiễm với HCV, HIV, HDV), về lâm sàng (có xơ gan) và về môi trường và lối sống (phơi nhiễm với Aflatoxin, nghiện rượu nặng, hút thuốc lá).
– HCV: theo số liệu của Tổ chức Y tế Thế giới (WHO) năm 2016, dựa trên một số nghiên cứu từ 2003 đến 2014, tỉ lệ nhiễm HCV ở người lớn tại Việt Nam khoảng 1-3,3%. Một phân tích gộp trên một số nghiên cứu bệnh-chứng (case-control studies) cho thấy người có kháng thể kháng HCV có nguy cơ bị UTBMTBG gấp 17 lần so với người không có kháng thể kháng HCV.
– Đồng nhiễm HBV và HCV: làm tăng nguy cơ bị UTBMTBG. Trong một nghiên cứu 24091 trường hợp UTBMTBG tại miền Trung và miền Nam Việt Nam trong thời gian 2010 đến 2016, tỉ lệ đồng nhiễm HBV và HCV là 2,7%.
– Sử dụng đồ uống có cồn: một phân tích gộp trên 19 nghiên cứu tiến cứu ghi nhận nguy cơ UTBMTBG tăng 16% ở những người sử dụng từ 3 đơn vị đồ uống có cồn trở lên mỗi ngày và tăng 22% ở những người sử dụng từ 6 đơn vị đồ uống có cồn trở lên mỗi ngày, và nguy cơ này cũng tăng ngay cả khi chỉ sử dụng lượng cồn thấp nhất mỗi ngày (25g mỗi ngày, tương ứng với 2 đơn vị đồ uống có cồn mỗi ngày). Ở Việt Nam, chưa có số liệu chính thức về mối liên quan giữa UTBMTBG và việc sử dụng đồ uống có cồn. Theo một nghiên cứu trên 1617 bệnh nhân UTBMTBG tại miền Trung và miền Nam Việt Nam, có 68,6% bệnh nhân đã và đang sử dụng đồ uống có cồn với nhiều mức độ khác nhau.
1.3. Phòng ngừa UTBMTBG
– Nên sử dụng vaccin chủng ngừa HBV cho trẻ em, nhất là trẻ sơ sinh để ngăn ngừa việc nhiễm HBV. Nên điều trị lâu dài và hiệu quả cho các bệnh nhân nhiễm HBV mạn và có bệnh lý gan đang hoạt động.
– Nên điều trị viêm gan virus C cho đến khi bệnh nhân đạt được đáp ứng virus bền vững (sustained virologic response – SVR). Nguy cơ UTBMTBG sẽ giảm đáng kể nếu các bệnh nhân viêm gan virus C mạn đạt được SVR. Tuy nhiên, ngay cả khi đạt được SVR, các bệnh nhân lớn tuổi, số lượng tiểu cầu thấp, và/hoặc có xơ gan vẫn có nguy cơ UTBMTBG cao và cần được tầm soát.
– Nên điều trị các bệnh lý chuyển hóa như bệnh gan nhiễm mỡ không do rượu (Non-alcoholic Fatty Liver Disease – NAFLD), bệnh viêm gan thoái hóa mỡ không do rượu (Non-alcoholic Steatohepatitis – NASH) vì các bệnh lý này làm tăng nguy cơ UTBMTBG, nhất là khi đã có xơ gan. Các hội chứng chuyển hóa, đặc biệt là tiểu đường và béo phì, làm tăng nguy cơ UTBMTBG trên các bệnh nhân bị NASH.
2. TẦM SOÁT UTBMTBG
2.1. Đối tượng tầm soát
– Nhóm nguy cơ cao: các trường hợp nhiễm HBV mạn và HCV mạn chưa điều trị, đang điều trị và đã ngưng điều trị bằng thuốc kháng virus, và các trường hợp xơ gan không liên quan đến nhiễm virus viêm gan.
– Nhóm nguy cơ rất cao: các trường hợp xơ gan có liên quan đến viêm gan do virus (HBV, HCV).
2.2. Phương tiện và tần suất tầm soát
– Tầm soát bằng siêu âm bụng và xét nghiệm phối hợp các chỉ dấu sinh học AFP, AFP-L3, PIVKA II.
– Tầm soát mỗi 6 tháng đối với nhóm nguy cơ cao và mỗi 3 tháng đối với nhóm nguy cơ rất cao. Nếu phát hiện có tổn thương nghi ngờ UTBMTBG và/hoặc giá trị các chỉ dấu sinh học tăng thì nên chụp CT scan bụng có cản quang hoặc MRI bụng có tương phản từ.
3. CHẨN ĐOÁN UTBMTBG
3.1. Khám lâm sàng và các xét nghiệm cận lâm sàng cần làm
– Cần tìm hiểu các yếu tố nguy cơ của bệnh nhân:
+ Bệnh nhân đã từng bị nhiễm hay đã hoặc đang điều trị nhiễm HBV và/hoặc HCV.
+ Gia đình bệnh nhân (cha mẹ, vợ chồng, anh chị em ruột) có người đã từng bị nhiễm hay đã hoặc đang điều trị nhiễm HBV và/hoặc HCV, hoặc đã được chẩn đoán bị UTBMTBG.
+ Đã từng được truyền máu hay từng sử dụng kim tiêm chung với người khác.
+ Tình trạng sử dụng thức uống có cồn (số lượng, tần suất, thời gian, …).
+ Đã từng tiếp xúc với các loại độc tố hay hóa chất (loại, thời gian tiếp xúc…).
+ Lý do đến khám bệnh (đau bụng, vàng da, bụng to, … hay chỉ là kiểm tra sức khỏe).
+ Các bệnh lý khác đi kèm (nếu có).
– Khám lâm sàng:
+ Phần lớn các trường hợp UTBMTBG chỉ có đau bụng mơ hồ hoặc được phát hiện tình cờ.
+ Đánh giá toàn trạng, dấu hiệu sinh tồn, tình trạng vàng da niêm mạc.
+ Khám tổng thể, khám bụng, chú ý có sờ thấy gan to hay không.
– Các xét nghiệm cận lâm sàng cần làm:
+ Công thức máu, chức năng đông máu toàn bộ, đường huyết.
+ Chức năng gan thận: ALT, AST, Bilirubin, Albumin, Ure, Creatinin máu.
+ Các xét nghiệm miễn dịch về virus viêm gan B, C: HBsAg, AntiHCV
+ Chỉ dấu sinh học của UTBMTBG: AFP, AFP-L3, PIVKA II (DCP).
+ Các chỉ dấu ung thư khác (nếu cần): CEA, CA 19.9, PSA, CA 12.5, … + X quang phổi thẳng.
+ Siêu âm Doppler mạch máu gan.
+ CT scan bụng có cản quang (và MRI bụng có tương phản từ nếu cần).
3.2. Hình ảnh học
3.2.1. Siêu âm
a. Siêu âm 2D và siêu âm Doppler mạch máu gan
Siêu âm 2D và siêu âm Doppler thuận tiện và có chi phí thấp nên là các phương tiện đầu tiên được áp dụng để tầm soát và theo dõi điều trị UTBMTBG, nhưng không dùng để chẩn đoán UTBMTBG. Siêu âm đánh giá hình dạng, vị trí, số lượng, kích thước khối u gan, tình trạng bệnh lý gan nền, tình trạng dịch ổ bụng và các tổn thương đi kèm trong ổ bụng. Siêu âm Doppler mạch máu gan cho phép đánh giá tình trạng cấp máu của khối u, tình trạng khối u xâm lấn và di căn vào các mạch máu lân cận, đặc biệt là tĩnh mạch cửa và tĩnh mạch chủ dưới.
Hệ thống Dữ liệu và Báo cáo hình ảnh Gan (The Liver Imaging Reporting and Data System – LI-RADS) khuyến cáo sử dụng siêu âm không tiêm chất tương phản để tầm soát và theo dõi UTBMTBG ở các bệnh nhân xơ gan và yếu tố nguy cơ cao khác.
b. Siêu âm có chất tương phản (contrast-enhanced ultrasound – CEUS)
Những thay đổi chính trong quá trình sinh UTBMTBG bao gồm sự hình thành mạch, thay đổi tế bào gan, giảm số lượng và chức năng của tế bào Kupffer, trong đó sự thay đổi huyết động của các nốt, bao gồm tăng lưu lượng động mạch và giảm lưu lượng tĩnh mạch cửa, là thay đổi quan trọng nhất để chẩn đoán UTBMTBG. Mật độ tế bào Kupffer giảm cùng với sự giảm biệt hóa của nốt xơ gan. Các vi bóng khí trong CEUS được thực bào bởi các tế bào Kupffer, nên hình ảnh tế bào Kupffer có thể quan sát được, các khối u ác tính có thể được phân biệt với vùng gan quanh u do chúng chứa ít hoặc không chứa tế bào Kupffer.
Hình ảnh điển hình của UTBMTBG trên CEUS là ngấm thuốc mạnh thì động mạch (arterial phase hyperenhancement – APHE) và thải thuốc nhẹ sau 60 giây. CEUS có độ nhạy cao để phát hiện tình trạng giảm quang thì động mạch và thể hiện tốt hơn dấu hiệu “thải thuốc” nhanh (diễn ra sớm, tại thời điểm 55-60 giây) đối với bệnh ác tính không phải UTBMTBG và “thải thuốc” rất muộn (sau 60 giây) đối với UTBMTBG. CEUS không có bức xạ ion hóa và các chất tương phản của CEUS không gây độc cho thận.
CEUS có phân độ theo LI-RADS được Hiệp hội Nghiên cứu Bệnh gan châu Á Thái Bình Dương (APASL) và Hội Ung thư Nội khoa châu Âu (ESMO) khuyến cáo dùng trong chẩn đoán UTBMTBG nhưng chưa được đồng thuận đưa vào các hướng dẫn chẩn đoán UTBMTBG khác trên thế giới do khó phân biệt được ung thư đường mật trong gan với UTBMTBG trong một số trường hợp. Bên cạnh đó, vẫn phải chỉ định CT và/hoặc MRI động để xác định giai đoạn bệnh trước khi điều trị.
3.2.2. Chụp cắt lớp vi tính (CT) và cộng hưởng từ (MRI)
Hình ảnh học đóng vai trò quan trọng trong chẩn đoán và trong việc đưa ra quyết định điều trị UTBMTBG nhờ vào việc mô tả đầy đủ hình thái gan và nêu lên được động học tưới máu gan. Tổn thương UTBMTBG có sự thay đổi điển hình là tăng nguồn cấp máu từ động mạch và giảm nguồn cấp máu từ tĩnh mạch cửa.
Để chẩn đoán UTBMTBG, cần có CT đa dãy đầu dò chụp đủ 4 thì và/hoặc MRI động có thì động mạch trễ, thì tĩnh mạch cửa và thì muộn (khoảng 3-5 phút sau khi tiêm chất tương phản từ). CT động và MRI động cho phép đánh giá mức độ phân bố mạch máu tại khối u, với hình ảnh điển hình của UTBMTBG là ngấm thuốc mạnh ở thì động mạch và thải thuốc ở thì tĩnh mạch cửa và/hoặc ở thì muộn.
MRI có thể phát hiện những khối u có kích thước nhỏ, nhất là các khối u < 2cm, dựa vào sự khảo sát trên nhiều chuỗi xung, đặc biệt là MRI động và chuỗi xung khuếch tán rất nhạy trong chẩn đoán. MRI cho phép chẩn đoán phân biệt rất tốt giữa UTBMTBG với các tổn thương khu trú khác trong gan như u máu, u tuyến (adenoma), tăng sinh dạng nốt khu trú (focal nodular hyperplasia-FNH), di căn gan hoặc nốt tân tạo trong xơ gan. Trong hầu hết các nghiên cứu về giá trị trong chẩn đoán UTBMTBG, MRI đều có độ nhạy cao hơn CT với độ chuyên biệt từ 85% đến 100%, đặc biệt đối với các tổn thương nhỏ. Các nghiên cứu gần đây khuyến cáo chụp MRI với chất tương phản từ gan-mật gadoxetate disodium (Gd-EOB-DTPA- gadolinium ethoxybenzyl diethylenetriamine pentaacetic acid) có độ nhạy cao hơn CT động và MRI sử dụng các chất tương phản từ khác.
Hình ảnh điển hình của UTBMTBG trên CT/MRI là giảm đậm độ ở thì chưa tiêm thuốc, ngấm thuốc mạnh ở thì động mạch (arterial phase hyperenhancement – APHE) và thải thuốc (wash-out) ở thì tĩnh mạch cửa hay thì muộn.
Ngoài giá trị chẩn đoán, CT/MRI còn được sử dụng để theo dõi và đánh giá sau điều trị UTBMTBG. Có thể sử dụng phân độ theo LI-RADS (Phụ lục 2 và 3) để hướng dẫn chẩn đoán và đánh giá kết quả điều trị.
Các tổn thương nghi ngờ là UTBMTBG nếu có ngấm lipiodol tại tổn thương sau khi làm Nút mạch hóa chất (TACE) thì được chẩn đoán là UTBMTBG.
3.2.3. PET và PET/CT
Chỉ có khoảng 40% các trường hợp UTBMTBG có hấp thu Fluorodeoxyglucose F 18 (18F) khi chụp PET và PET/CT, và hầu hết các trường hợp UTBMTBG biệt hóa cao đều cho kết quả âm tính khi chụp PET và PET/CT. Tuy nhiên, PET và PET/CT rất có giá trị để phát hiện các tổn thương di căn ngoài gan của UTBMTBG, nhất là trong các trường hợp không thấy tổn thương UTBMTBG mới hay tiến triển tại gan sau khi điều trị. Ngoài ra có thể chụp PET/CT với 11C-Choline để phát hiện tổn thương tại gan, ngoài gan tốt hơn 18F.
3.2.4. Các xét nghiệm khác
– Xạ hình xương bằng máy SPECT, SPECT/CT với 99mTc-MDP để đánh giá tổn thương di căn xương, chẩn đoán giai đoạn bệnh trước điều trị, theo dõi đáp ứng điều trị, đánh giá tái phát và di căn.
– Xạ hình thận chức năng bằng máy SPECT, SPECT/CT với 99mTc-DTPA để đánh giá chức năng thận trước điều trị và sau điều trị.
– Xạ hình – SPECT gan với 99mTc-Sulfure Colloid: hình ảnh khối choán chỗ trong gan, áp dụng trong một số trường hợp.
– Xạ hình gan mật trong một số trường hợp
3.3. Chỉ dấu sinh học
3.3.1. Alpha-fetoprotein (AFP)
Vai trò của AFP trong chẩn đoán UTBMTBG chưa rõ ràng. AFP có thể tăng trong các trường hợp viêm gan hoạt động và xơ gan, và có thể giảm đi khi điều trị các tình trạng viêm gan bằng các thuốc điều trị HBV và HCV. Ngưỡng giá trị bình thường của AFP thường là 20 ng/ml, ngưỡng giá trị chẩn đoán của AFP là 400 ng/ml. AFP có thể được sử dụng phối hợp với siêu âm để tầm soát UTBMTBG trên các đối tượng nguy cơ.
3.3.2. Lens culinaris agglutinin-reactive fraction of AFP (AFP-L3)
AFP-L3 có thể được dùng để phân biệt sự gia tăng AFP trong các trường hợp UTBMTBG với các trường hợp u lành tính ở gan. Ngưỡng giá trị bình thường của AFP-L3 là 5%.
3.3.3. Prothrombin induced by vitamin K absence-II (PIVKA II) hay còn gọi là Des-gamma-carboxyprothrombin (DCP)
PIVKA II là một prothombin bất thường, tăng trong huyết thanh của các trường hợp UTBMTBG. Ngưỡng giá trị bình thường của PIVKA II là 40 mAU/ml.
3.3.4. Một số chỉ dấu sinh học khác trong huyết thanh
Các chỉ dấu sinh học khác như Glypican-3 (GPC3), Golgi protein 73 (GP73), Osteopontin, circulating cell free DNA, và các microRNA chưa có vai trò rõ ràng về chuyên môn lẫn hiệu quả về kinh tế.
3.3.5. Kết hợp các chỉ dấu sinh học trong huyết thanh
Sự kết hợp các chỉ dấu sinh học AFP, AFP-L3 và PIVKA II trong huyết thanh có thể cải thiện độ nhạy trong tầm soát và chẩn đoán UTBMTBG mà không làm giảm đi độ chuyên biệt, do đó nên sử dụng việc kết hợp này trong thực tế lâm sàng.
3.4. Sinh thiết gan
Trong những trường hợp tổn thương ở gan không đáp ứng được các tiêu chuẩn chẩn đoán dưới đây thì sinh thiết gan cho phép xác định chẩn đoán UTBMTBG và phân biệt với các tổn thương ác tính nguyên phát khác tại gan như ung thư đường mật, ung thư gan-mật kết hợp, cũng như các tổn thương ác tính thứ phát tại gan các u thần kinh nội tiết và các tổn thương di căn tại gan. Các nguy cơ như chảy máu hay gieo rắc tế bào ung thư đều có tỉ lệ rất thấp, có thể xử trí được và không ảnh hưởng đến quyết định làm sinh thiết gan khi cần thiết.
Kết quả sinh thiết gan cần được đối chiếu với các dữ liệu về hình ảnh học và chỉ dấu sinh học để quyết định nên sinh thiết lại hay nên theo dõi tiếp. Nếu quyết định theo dõi tiếp thì nên đánh giá lại tổn thương bằng hình ảnh học và chỉ dấu sinh học sau 02 tháng.
3.5. Chẩn đoán xác định UTBMTBG
Khi tổn thương ở gan có một trong ba tiêu chuẩn sau:
– Hình ảnh điển hình* của UTBMTBG trên CT scan bụng có cản quang hoặc MRI bụng có tương phản từ + AFP ≥ 400 ng/ml.
– Hình ảnh điển hình* của UTBMTBG trên CT scan bụng có cản quang hoặc MRI bụng có tương phản từ + AFP tăng cao hơn bình thường (nhưng chưa đến 400 ng/ml) + có nhiễm HBV và/hoặc HCV. Có thể làm sinh thiết gan để chẩn đoán xác định nếu bác sĩ lâm sàng thấy cần thiết.
Các trường hợp không đủ các tiêu chuẩn nói trên đều phải làm sinh thiết khối u gan (có thể phải làm nhiều lần) để chẩn đoán xác định. Nếu sinh thiết lại vẫn âm tính thì có thể theo dõi và làm lại các xét nghiệm hình ảnh học và chỉ dấu sinh học mỗi 2 tháng.
– Có bằng chứng giải phẫu bệnh lý là UTBMTBG.
* Hình ảnh điển hình trên CT scan bụng có cản quang hoặc MRI bụng có tương phản từ: khối u bắt thuốc trên thì động mạch gan và thải thuốc (wash-out) trên thì tĩnh mạch cửa hay thì chậm. Nên chụp MRI với chất tương phản từ gan – mật gadoxetate disodium (Gd-EOB-DTPA – gadolinium ethoxybenzyl diethylenetriamine pentaacetic acid) để tăng khả năng chẩn đoán ung thư biểu mô tế bào gan.
Sơ đồ chẩn đoán UTBMTBG
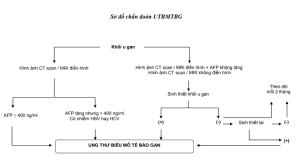
3.6. Chẩn đoán phân biệt
– U máu ở gan (hemangioma): khối u bắt thuốc tăng dần từ thì động mạch gan đến thì chậm trên CT scan hoặc MRI, chỉ dấu sinh học của UTBMTBG bình thường, có thể có hoặc không nhiễm HBV và/hoặc HCV.
– Các u lành ở gan như u tuyến (adenoma), tăng sinh dạng nốt (focal nodular hyperplasia – FNH), áp xe gan, nốt vôi hóa ở gan, …: hình ảnh không điển hình trên CT scan hoặc MRI, chỉ dấu sinh học của UTBMTBG bình thường, có thể có hoặc không nhiễm HBV và/hoặc HCV, có thể xác định nhờ MRI bụng có tương phản từ đặc hiệu hoặc sinh thiết gan.
– Ung thư đường mật trong gan: khối u bắt thuốc không đồng đều, không có hiện tượng thải thuốc, chỉ dấu ung thư CEA, CA 19.9 có thể tăng cao. Chẩn đoán xác định nhờ sinh thiết gan.
– Di căn gan của các ung thư khác (ung thư dạ dày, ung thư đại trực tràng, ung thư phổi, ung thư vú, …): hình ảnh bắt thuốc dạng viền trên CT scan hoặc MRI, các chỉ dấu ung thư tương ứng tăng cao, có tổn thương nguyên phát, …
3.7. Phân chia giai đoạn bệnh
Các Hướng dẫn điều trị của Nhóm Ung thư gan Barcelona (BCLC), Hội Nghiên cứu bệnh gan châu Âu (EASL), Hội Ung thư Nội khoa châu Âu (ESMO) và Hội Nghiên cứu bệnh gan Hoa Kỳ (AASLD) phân chia UTBMTBG thành 5 giai đoạn bệnh: 0 (rất sớm), A (sớm), B (trung gian), C (tiến triển), D (cuối), để đề ra cách điều trị phù hợp. Trong khi đó, Hiệp hội nghiên cứu bệnh gan châu Á Thái Bình Dương (APASL) không phân chia giai đoạn bệnh, mà dựa trên 6 yếu tố: di căn ngoài gan, chức năng gan (đánh giá bằng hệ thống Child-Pugh), khả năng cắt gan được, xâm nhập mạch máu lớn, số lượng u, kích thước u, để chọn lựa các điều trị phù hợp.
Bệnh viện Đa khoa Quốc tế Vinmec đã đưa hệ thống máy móc, thiết bị hiện đại đạt chuẩn vào công tác thăm khám, chẩn đoán, gây mê và điều trị các bệnh lý liên quan đến gan. Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Nguồn: GLOBOCAN. Bộ Y tế, “Hướng dẫn chẩn đoán và điều trị ung thư biểu mô tế bào gan”
Leave a Reply