Thuyên tắc phổi (PE) cấp tính vẫn là một trong những nguyên nhân hàng đầu gây tử vong cho sản phụ ở các quốc gia thu nhập cao. Ví dụ, ở Anh và Ireland, huyết khối và thuyên tắc huyết khối là nguyên nhân tử vong mẹ trực tiếp phổ biến nhất (tử vong do mang thai chứ không phải do các bệnh lý trước đó) trong 3 năm từ 2013-2015, dẫn đến tử vong 1.13 trên 100 000 bà mẹ.
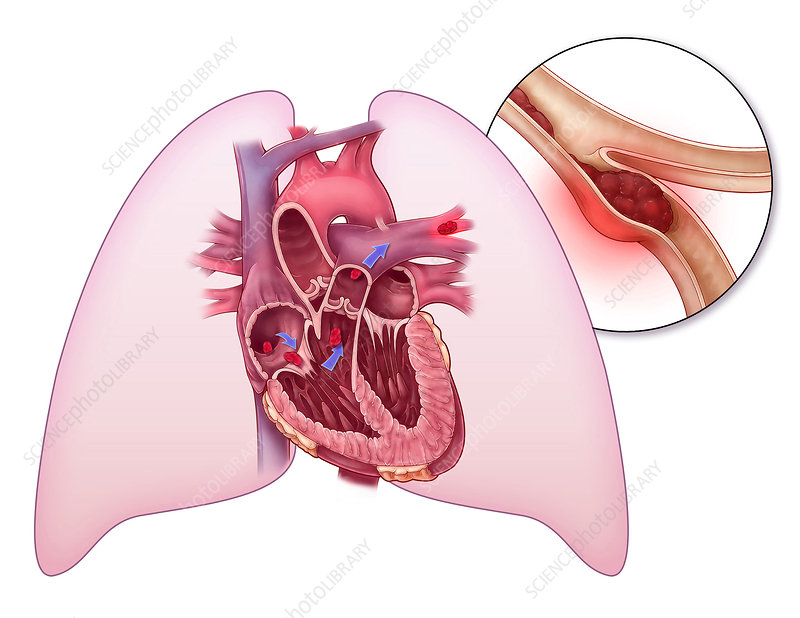
1. Dịch tễ học và các yếu tố nguy cơ thuyên tắc phổi trong thai kỳ
Nguy cơ VTE cao hơn ở phụ nữ mang thai so với phụ nữ không mang thai trong cùng độ tuổi; nguy cơ tăng lên trong thai kỳ và đạt đến đỉnh điểm trong giai đoạn sau sinh. Nguy cơ nền liên quan đến mang thai gia tăng hơn nữa nếu có mặt các yếu tố nguy cơ VTE đi kèm, kể cả thụ tinh trong ống nghiệm: trong một nghiên cứu cắt ngang bắt nguồn từ một đăng bộ Thụy Điển, HR cho VTE sau thụ tinh trong ống nghiệm là 1.77 (95% CI 1.41- 2.23) tổng thời gian và 4.22 (95% CI 2.46-7.20) trong ba tháng đầu tiên. Các yếu tố nguy cơ quan trọng và phổ biến khác bao gồm từng bị VTE, béo phì, bệnh lý đi kèm, thai chết lưu, tiền sản giật, xuất huyết sau sinh, và mổ lấy thai; đánh giá nguy cơ từng được ghi nhận trước đây là rất quan trọng.
Các khuyến cáo được cung cấp trong các phác đồ này phù hợp với những điều được đưa vào Hướng dẫn ESC 2018 về quản lý bệnh tim mạch trong thai kỳ.
2. Chẩn đoán
2.1 Quy tắc dự đoán lâm sàng và D-dimer
Chẩn đoán PE khi mang thai có thể khó khăn vì các triệu chứng thường trùng lặp với những thai kỳ bình thường. Tỷ lệ bệnh nhân được chẩn đoán xác định PE là thấp trong số phụ nữ nghi ngờ mắc bệnh, từ 2 đến 7%. Nồng độ D-dimer tăng liên tục trong thai kỳ, và nồng độ cao hơn ngưỡng loại trừ VTE gặp trong gần một phần tư phụ nữ mang thai trong tam cá nguyệt thứ ba. Kết quả của một nghiên cứu tiến cứu đa quốc gia về xử trí trên 441 phụ nữ mang thai đến khoa cấp cứu với lâm sàng nghi ngờ PE cho thấy rằng một chiến lược chẩn đoán – dựa trên đánh giá xác suất lâm sàng, đo D-dimer, CUS và CTPA – có thể loại trừ an toàn PE trong thai kỳ. Trong nghiên cứu đó, việc loại trừ PE dựa trên cơ sở kết quả D-dimer âm tính (không có hình ảnh) là khả thi ở 11.7% trong số 392 phụ nữ có Điểm xác suất trước cận lâm sàng (Geneva) không cao, tỷ lệ này giảm xuống còn 4.2% trong tam cá nguyệt thứ ba. Một nghiên cứu tiến cứ xa hơn về xử trí đánh giá sự kết hợp giữa lưu đồ điều chỉnh theo thai kỳ YEARS với nồng độ D-dimer ở 498 phụ nữ nghi ngờ PE khi mang thai. PE đã được loại trừ mà không có CTPA ở phụ nữ được coi là có nguy cơ PE thấp theo sự kết hợp của lưu đồ và kết quả D-dimer. Sau 3 tháng, chỉ có một phụ nữ đã loại trừ PE dựa trên lưu đồ là tiến triển DVT khoeo (0.21%, 95% CI 0.04-1.2) và không có phụ nữ nào tiến triển PE.
2.2. Chẩn đoán hình ảnh
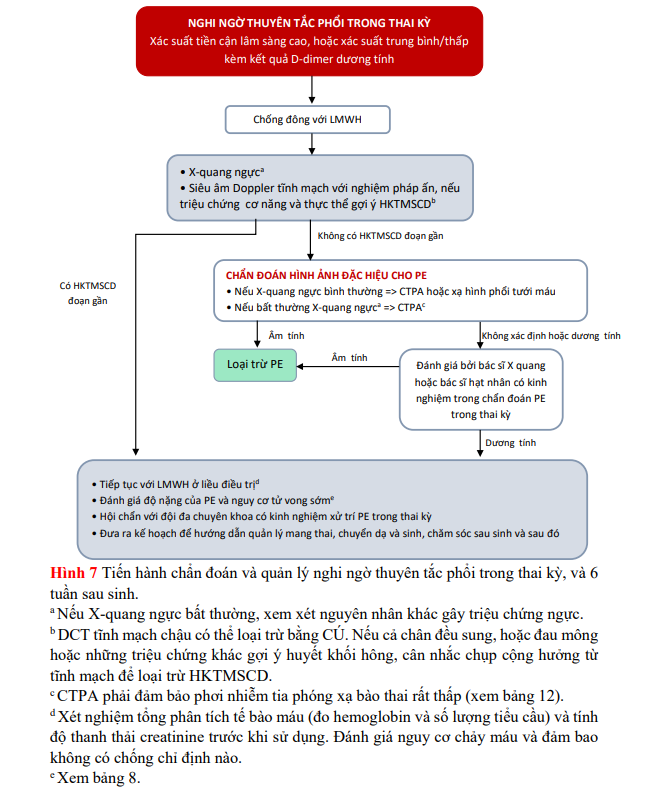
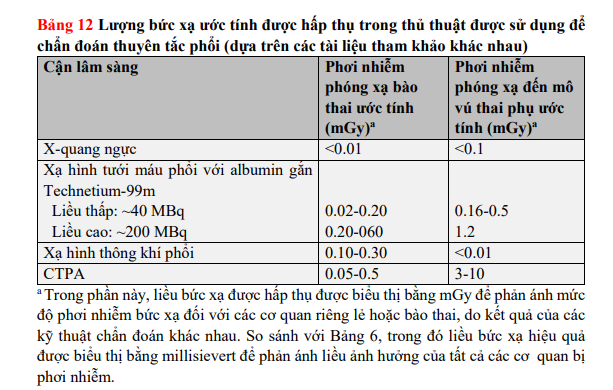
Một lưu đồ đề xuất cho việc chẩn đoán khi nghi ngờ PE ở phụ nữ mang thai, hoặc ≤6 tuần sau sinh, được hiển thị trong Hình 7. Cả phơi nhiễm bức xạ của mẹ và thai đều thấp khi sử dụng các kỹ thuật hình ảnh hiện đại (Bảng 12). Đối với xạ hình V/Q và CTPA, liều bức xạ của thai nhi thấp hơn nhiều so với ngưỡng biến chứng liên quan đến phóng xạ của thai nhi (là 50-100 mSv). Trước đây, CTPA đã được báo cáo gây ra phơi nhiễm bức xạ cao đến mô vú; tuy nhiên, công nghệ CT đã phát triển và một số kỹ thuật có thể giảm phơi nhiễm với bức xạ mà không ảnh hưởng đến chất lượng hình ảnh. Những kỹ thuật này bao gồm giảm phạm vi giải phẫu khi quét, giảm Kilo điện thế, sử dụng các kỹ thuật dựng hình lặp lại, và giảm bớt thì theo dõi cản quang của CTPA (CTPA có 3 thì: định khu bệnh nhân, theo dõi cản quang, scan chẩn đoán). Kỹ thuật hình ảnh CTPA hiện đại có thể phơi nhiễm mô vú của mẹ với liều trung bình thấp tới mức 3-4 mGy (Bảng 12). Ảnh hưởng đến nguy cơ ung thư của mẹ với kỹ thuật CTPA hiện đại là không đáng kể (nguy cơ ung thư suốt đời được báo cáo tăng theo hệ số 1.0003-1.0007); vì thế tránh sử dụng CTPA vì lý do nguy cơ ung thư của mẹ là không chính đáng.
Hình ảnh xạ hình tưới máu bình thường và CTPA âm tính là an toàn như nhau để loại trừ PE trong thai kỳ, như được đề xuất bằng loạt nghiên cứu hồi cứu. Kết quả không kết luận có thể là một vấn đề (4-33% lần chụp), đặc biệt là vào cuối thai kỳ. Một cuộc khảo sát gần đây tại 24 địa điểm ở Anh, đại diện cho một dân số 15.5 triệu người, cho thấy tỷ lệ CTPA và xạ hình không hợp lý hoặc không xác định là gần như nhau, điều này gợi ý rằng lựa chọn phương tiện chẩn đoán hình ảnh ban đầu tốt nhất nên tùy thuộc vào chuyên môn và nguồn lực của bệnh viện.
V/Q SPECT có liên quan đến phơi nhiễm bức xạ thai nhi và mẹ thấp và hứa hẹn trong chẩn đoán PE thai kỳ. Tuy nhiên, đánh giá thêm về kỹ thuật này là cần thiết trước khi đưa rộng rãi vào các lưu đồ chẩn đoán. Đối với MRA, tác dụng lâu dài của chất tương phản gadolinium đối với thai nhi chưa được biết đến. Ở những bệnh nhân không mang thai, MRA thường thu được hình ảnh không chuẩn về mặt kỹ thuật và tỷ lệ cao kết quả không kết luận được. Do đó, sử dụng kỹ thuật này để chẩn đoán hoặc loại trừ PE trong quá trình mang thai hiện nay không được khuyến cáo. Chụp động mạch phổi cổ điển liên quan đến phơi nhiễm phóng xạ cao hơn đáng kể đến thai nhi (2.2-3.7 mSv) và nên tránh trong thời gian mang thai.
Chẩn đoán quá tay PE là một cạm bẫy tiềm ẩn có thể ảnh hưởng quan trọng và suốt đời đối với một thai phụ, bao gồm cả nguy cơ chảy máu tại thời điểm sinh nở, việc tạm ngưng tránh thai bằng estrogen và yêu cầu điều trị dự phòng huyết khối trong những lần mang thai kế tiếp. Do đó, tránh chẩn đoán PE quá tay trong thai kỳ là quan trọng tương đương như việc không bỏ sót chẩn đoán PE.
2.3 Điều trị PE trong thai kỳ
LMWH là lựa chọn điều trị thuyên tắc phổi khi mang thai. Trái ngược với VKA và NOAC, LMWH không qua nhau thai và do đó không gây nguy cơ xuất huyết thai nhi hoặc gây quái thai. Hơn nữa, mặc dù UFH cũng an toàn trong thai kỳ, nhưng LMWH có dược động học dễ dự đoán hơn và ít nguy cơ hơn. Mặc dù chưa có RCT đánh giá liều tối ưu của LMWH để điều trị PE trong thai kỳ, dữ liệu hiện được công bố ủng hộ liều tương tự cho bệnh nhân không mang thai, với phương thức o.d. hoặc b.i.d. dựa trên cân nặng lúc đầu thai kỳ. Đối với phần lớn bệnh nhân được điều trị LMWH cho PE trong thai kỳ, vẫn không chắc chắn liệu đo hàng loạt hoạt độ kháng yếu tố X huyết tương để hướng dẫn dùng thuốc có lợi ích lâm sàng gì không. Điều quan trọng là phải nhớ rằng:
(i) LMWH có dược động học dự đoán được,
(ii) Thiếu dữ liệu về nồng độ tối ưu kháng yếu tố đông máu hoạt hóa,
(iii) Bản thân xét nghiệm cũng có những hạn chế. Ngoài ra, không có dữ liệu vững chắc về lợi ích lâm sàng so với tác hại của việc điều chỉnh liều thường xuyên, dựa trên cân nặng của LMWH khi mang thai. Do đó, theo dõi nồng độ kháng yếu tố đông máu X hoạt hóa có thể được dành riêng cho các trường hợp nguy cơ cao cụ thể như VTE tái phát, suy thận và trọng lượng cơ thể quá nhỏ hoặc quá lớn.
Việc sử dụng UFH có liên quan đến giảm tiểu cầu do heparin và mất xương. Vẫn không chắc chắn nguy cơ mất xương tăng lên khi sử dụng LMWH ở mức độ nào. Trong một nghiên cứu quan sát đoàn hệ gần đây, mật độ xương được đo bằng phương pháp hấp phụ tia X năng lượng kép 4-7 năm sau lần sinh nở cuối cùng ở 152 phụ nữ (92 người trong số họ có điều trị LMWH kéo dài khi mang thai), mật độ xương cột sống thắt lưng là tương tự giữa nhóm được điều trị bằng LWMH và nhóm chứng sau khi điều chỉnh cho các yếu tố có khả năng gây nhiễu. Không có loãng xương hoặc gãy xương do loãng xương được báo cáo.
Có thể xem xét fondaparinux thay thế nếu có dị ứng hoặc đáp ứng bất lợi với LMWH, mặc dù còn thiếu dữ liệu vững chắc và có qua hàng rào nhau thai lượng ít. VKA qua nhau thai và liên quan đến bệnh lý phôi thai trong tam cá nguyệt đầu tiên. Cho VKA trong tam cá nguyệt thứ ba có thể dẫn đến xuất huyết thai nhi và xuất huyết sơ sinh, cũng như bong nhau. Warfarin có thể liên quan đến dị thường hệ thần kinh trung ương trong bào thai trong suốt thai kỳ. NOAC là chống chỉ định ở bệnh nhân mang thai.
Việc xử trí chuyển dạ và sanh đòi hỏi sự chú ý đặc biệt. Ở phụ nữ đang điều trị LMWH, cần xem xét sanh chương trình với phối hợp nhóm nhiều chuyên khoa để tránh nguy cơ chuyển dạ tự nhiên khi đã chống đông hoàn toàn. Tỷ suất hiện mắc hematoma tủy sống sau khi gây tê vùng ở phụ nữ mang thai đang điều trị chống đông là không rõ. Nếu xem xét giảm đau vùng ở một phụ nữ đang điều trị LMWH, cần chờ ≥24h kể từ liều LMWH cuối cùng trước khi đâm kim tê tủy sống hoặc kim tê ngoài màng cứng (giả sử chức năng thận bình thường và đã đánh giá nguy cơ nếu trọng lượng cơ thể quá thấp hoặc quá cao).
Trong các tình huống nguy cơ cao, ví dụ ở những bệnh nhân mắc thuyên tắc phổi gần đây, LMWH được khuyến cáo nên đổi thành UFH ≥36 giờ trước sanh. Nên ngừng truyền UFH 4-6 giờ trước khi sinh dự kiến và thời gian thromboplastin hoạt hóa một phần trở về bình thường (tức là không kéo dài) trước khi gây tê vùng.
Dữ liệu hiện có về thời gian tối ưu hóa khởi động lại LMWH sau sinh thì hạn chế. Thời gian sẽ phụ thuộc vào phương pháp sanh và đánh giá lợi hại giữa nguy cơ huyết khối và nguy cơ chảy máu bởi nhóm đa chuyên khoa. Không nên cho LMWH cho đến khi ≥4 giờ sau khi lấy catheter ngoài màng cứng; quyết định về thời gian và liều lượng nên xem xét liệu lúc đưa catheter vào khoang ngoài màng cứng có tổn thương gì hay không, và tính đến các yếu tố nguy cơ của người phụ nữ. Ví dụ, một liều tạm thời LMWH dự phòng có thể cân nhắc cho khi hậu phẫu (sau khi mổ lấy thai), ít nhất 4 giờ sau khi catheter ngoài màng cứng được lấy ra và cho phép một khoảng ≥8-12 giờ giữa liều dự phòng và liều điều trị tiếp theo. Phối hợp chặt chẽ giữa bác sĩ sản khoa, bác sĩ gây mê và bác sĩ điều trị chính được khuyến cáo.
Điều trị chống đông máu nên được dùng tiếp ≥6 tuần sau khi sinh và với tổng thời gian điều trị tối thiểu là 3 tháng. LMWH và warfarin có thể được dùng cho các bà mẹ cho con bú; việc sử dụng NOAC không được khuyến cáo.
PE nguy cơ cao, đe dọa tính mạng khi mang thai là một sự kiện hiếm gặp nhưng rất trầm trọng. Một tổng quan hệ thống gần đây bao gồm 127 trường hợp PE nặng khi mang thai (và cho đến 6 tuần sau sinh) được điều trị bằng tiêu sợi huyết, lấy huyết khối và/hoặc ECMO. Trong đó bao gồm các trường hợp PE nguy cơ cao và trung bình, và 23% phụ nữ có ngừng tim. Tỷ lệ sống sót được báo cáo là 94 và 86% tương ứng với sau khi tiêu sợi huyết và phẫu thuật lấy huyết khối; tuy nhiên, các tỷ lệ cao này có thể phản ánh sai số trong báo cáo. Khi dùng tiêu sợi huyết, chảy máu lớn xảy ra ở 18% các trường hợp trong thời kỳ mang thai và 58% trong giai đoạn sau sinh. Cuối cùng, thai chết xảy ra ở 12 và 20% lần lượt các trường hợp sau tiêu sợi huyết và lấy huyết khối. Điều trị tiêu sợi huyết không nên được sử dụng chu sanh, ngoại trừ trong trường hợp PE đe dọa tính mạng. Thông thường, UFH được sử dụng trong điều trị PE cấp tính nguy cơ cao.
Mặc dù các chỉ định cho lưới lọc tĩnh mạch chủ tương tự như bệnh nhân không mang thai, tuy nhiên kinh nghiệm sử dụng lưới lọc trong thai kỳ không nhiều, vì thế nguy cơ liên quan đến thủ thuật có thể tăng lên.
- Vai trò của một nhóm đa chuyên khoa về bệnh lý tim trong thai kỳ
Một nhóm các đồng nghiệp đa chuyên khoa nên hợp tác trong việc lập kế hoạch các lộ trình chăm sóc trước, trong và sau sinh cho phụ nữ có bệnh tim mạch, bao gồm PE. Càng nhiều thành viên của nhóm này nên có chuyên môn về quản lý PE khi mang thai và thời kỳ hậu sản thì càng tốt. Nên có sẵn văn bản đồng ý hợp tác, và phác đồ hướng dẫn chăm sóc cũng nên có sẵn (nếu thời gian cho phép) để giao tiếp hiệu quả.
2.4. Thuyên tắc ối
Thuyên tắc ối (AFE) là một tình trạng hiếm gặp xảy ra trong thai kỳ hoặc ngay sau khi sinh. Nó vẫn là một trong những nguyên nhân tử vong mẹ trực tiếp hàng đầu (nghĩa là tử vong do mang thai chứ không phải do các điều kiện tồn tại từ trước) ở các quốc gia thu nhập cao. Chẩn đoán AFE là một thách thức, chủ yếu là chẩn đoán lâm sàng loại trừ. Nhận thức về AFE, chẩn đoán kịp thời và hồi sức tim phổi tích cực là rất quan trọng. AFE đặc trưng bởi trụy tim mạch hoặc suy hô hấp đột ngột không giải thích được, thường đi kèm với đông máu nội mạch lan tỏa, xảy ra lúc mang thai hoặc sau khi sinh. Tỷ suất phát sinh được báo cáo là khoảng 2-7 trên 100 000 bà mẹ với tỷ suất tử vong 0.5-6 người chết trên 100 000 cuộc sanh. Tỷ lệ tử vong trên số ca mắc thuyên tắc ối được báo cáo khác nhau, phản ánh những thách thức trong việc chẩn đoán và sự hiếm gặp của AFE.
Trong một nghiên cứu hồi cứu ở California bao gồm hơn 3.5 triệu ca sanh, tỷ lệ tử vong trên số ca mắc thuyên tắc ối được báo cáo là 13%, như những nghiên cứu ở nơi khác của Hoa Kỳ và Canada. Tương tự, tỷ lệ tử vong trên số ca mắc thuyên tắc ối là 19% được báo cáo trong một nghiên cứu tiến cứu gần đây dựa trên dân số của Anh với tiêu chí xác thực các trường hợp. Tài liệu gần đây đã cho rằng các yếu tố nguy cơ của AFE có thể bao gồm bệnh tim, mạch máu não, và bệnh thận trước đó, nhau tiền đạo, đa ối, thai chết lưu, viêm màng đệm, rối loạn tăng huyết áp, sinh bằng dụng cụ, và sinh mổ. Quản lý AFE là hỗ trợ, và dựa trên chăm sóc cấp cứu chất lượng cao sau khi tình trạng được nhận ra và chẩn đoán, với điều trị chảy máu và rối loạn đông máu kịp thời. Nhận thức về AFE nên phối hợp với giáo dục các bác sĩ liên quan và các lưu đồ cấp cứu.
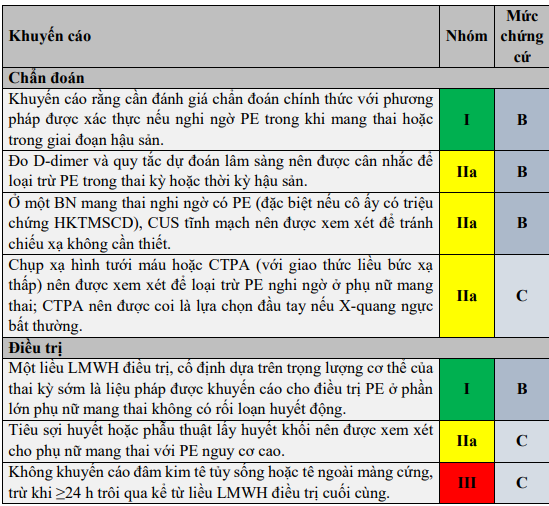
2.5 Khuyến cáo thuyên tắc phổi trong thai kỳ

Xem thêm:
Thuyên tắc động mạch phổi trong thực hành lâm sàng (vinmecdr.com)
Video đề xuất:
Các giai đoạn chuyển dạ từ cơn co đến khi sinh?
Tài liệu tham khảo:
Leave a Reply