Daprodustat được phát triển để thay thế cho phương pháp điều trị truyền thống bằng EPO, giúp giảm tải cho bệnh nhân và cải thiện chất lượng cuộc sống khi chứng minh được hiệu quả trong điều trị thiếu máu
1.Giới thiệu chung
Thiếu máu của bệnh thận mạn tính (CKD) là một biến chứng phổ biến trong bệnh thận mạn tính, thường để lại các biến chứng xấu và làm tăng nguy cơ tử vong. Thiếu máu thường đường định nghĩa là khi huyết sắc tố < 13,0g/dL ở nam giới và < 12,0g/dL ở phụ nữ. Theo thống kê ước tính có khoảng 14,0% dân số trưởng thành ở Hoa Kỳ mắc CKD trong năm 2007–2010. Thiếu máu phổ biến gấp đôi ở những người bị CKD (15,4%) so với những người khỏe mạnh (7,6%). Tỷ lệ thiếu máu tăng theo giai đoạn bệnh thận mạn, từ 8,4% ở giai đoạn 1 lên 53,4% ở giai đoạn 5
Thận có chức năng lọc máu, loại bỏ các chất thải và kiểm soát sự cân bằng của chất lỏng và chất điện giải trong cơ thể. Quá trình lọc xảy ra thông qua các bó mao mạch được gọi là cầu thận (số ít, cầu thận). Mức lọc cầu thận (GFR) giảm xuống < 60 mL/phút/1,73m2 cho thấy bệnh thận mãn tính (CKD). Ngoài ra, một trong những chức năng ít được biết đến của thận là sản xuất Erythropoietin để đáp ứng với tình trạng giảm nồng độ oxy trong máu
Nguyên nhân gây thiếu máu của bệnh thận mạn tính (CDK) bao gồm: thiếu sắt, viêm và tích tụ độc tố ure, nhiễm trùng, suy dinh dưỡng
Khi rơi vào tình trạng thiếu máu của bệnh thận mạn tính (CDK) có thể gây ra một số triệu chứng như sau: mệt mỏi, hụt hơi, da nhợt nhạt bất thường, nhức mỏi cơ thể, đau ngực, chóng mặt, ngất xỉu, nhịp tim nhanh hoặc không đều, nhức đầu, vấn đề về giấc ngủ, khó tập trung
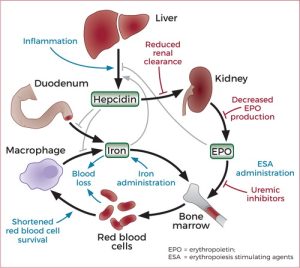
Thiếu máu do bệnh thận mạn tính (ACD) là nguyên nhân phổ biến nhất gây thiếu máu ở bệnh nhân nhập viện.Thiếu máu do bệnh thận mạn tính được hình thành do sự kích hoạt hệ thống miễn dịch bởi các kháng nguyên tự động, phân tử vi sinh vật hoặc thông qua hoạt động của yếu tố hoại tử khối u (TNF) và Interleukin (IL)-1 ,IL-6 và Interferon (IFN). Các cytokine này, cũng như hepcidin protein giai đoạn cấp tính, được cho là có tác dụng ức chế giải phóng sắt từ các đại thực bào tủy đến các tế bào tiền thân hồng cầu. Các cytokine cũng trực tiếp tạo ra sự điều hòa dịch mã/phiên mã của các gen liên quan đến cân bằng nội môi Sắt trực tiếp hoặc thông qua việc sản xuất các gốc không bền. Cụ thể, sự xâm nhập của vi sinh vật, khối u ác tính và rối loạn tự miễn dịch gây ra sự kích hoạt tế bào lympho T CD3 và đại thực bào giải phóng các cytokine – IFN-γ (từ tế bào T), TNF-α, IL-1 và −6. Các cytokine ức chế sự biểu hiện của Ferroportin 1 làm giảm quá trình vận chuyển Sắt từ đại thực bào sang các tiền chất hồng cầu đang phát triển
2.Thông tin thuốc về viên nén Jesduvroq (Daprodustat)
Đầu năm 2023, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đã phê duyệt Jesduvroq (Daprodustat) là phương pháp điều trị bằng đường uống đầu tiên cho bệnh thiếu máu do bệnh thận mãn tính gây ra cho người lớn đã được lọc máu ít nhất 4 tháng trong khi các phương pháp điều trị khác được FDA chấp thuận cho tình trạng này là tiêm vào máu hoặc dưới da. Hiệu quả của Jesduvroq đã được thiết lập trong một nghiên cứu ngẫu nhiên trên 2.964 người trưởng thành được lọc máu. Trong nghiên cứu này, những người trưởng thành được uống Jesduvroq hoặc tiêm Erythropoietin tổng hợp và kết quả từ nghiên cứu cho thấy Jesduvroq đã tăng và duy trì huyết sắc tố tương tự với Erythropoietin tổng hợp ở người.

2.1 Nhóm dược lý và chỉ định sử dụng
Daprodustat là một chất ức chế enzyme prolyl hydroxylase (HIF-PHI) gây thiếu oxy được chỉ định để điều trị bệnh thiếu máu do bệnh thận mãn tính ở người lớn đã được lọc máu ít nhất 4 tháng. Daprodustat không giúp cải thiện chất lượng cuộc sống, sự mệt mỏi hoặc sức khỏe của bệnh nhân và không được khuyến cáo sử dụng để thay thế cho việc truyền máu ở những bệnh nhân cần điều chỉnh tình trạng thiếu máu ngay lập tức.
2.2 Cơ chế hoạt động
Khi cơ thể thiếu oxy (khi lên cao) sẽ kích thích sản xuất EPO để tăng hồng cầu và khôi phục lại sự cân bằng oxy. Cơ chế bù trừ này được bắt đầu thông qua đồng dạng HIF-α được gọi là HIF-1. Khi HIF-α tích lũy và kết hợp với HIF-β để tạo thành một bộ điều chỉnh chức năng, sau đó HIF-α/β sẽ di chuyển vào nhân tế bào và liên kết với các yếu tố phản ứng thiếu oxy (HRE) trên ADN. Quá trình này dẫn đến tăng biểu hiện gen của EPO (Erythropoietin), một hormone được sản xuất bởi thận và có chức năng kích thích sản xuất hồng cầu trong cơ thể. Cuối cùng, quá trình tạo hồng cầu được tăng lên, quá trình vận chuyển sắt được điều hòa lại và nồng độ Hb trong tuần hoàn tăng lên
2.3 Dược động học
Hấp thu: Nồng độ ở trạng thái ổn định đạt được trong vòng 24 giờ sau khi dùng thuốc. Sau khi uống, Daprodustat được hấp thu dễ dàng với thời gian trung bình để đạt được nồng độ tối đa (Tmax) ở ở những đối tượng khỏe mạnh là từ 1-4 giờ. Sinh khả dụng tuyệt đối của Daprodustat là 65%.
Phân bố: Daprodustat có sự phân bố xấp xỉ bằng nhau giữa huyết tương và tế bào máu. Sau khi dùng liều tiêm tĩnh mạch, thể tích phân bố (Vd) ở trạng thái ổn định ở những đối tượng khỏe mạnh là 14,3L. Sự gắn kết với protein huyết tương là > 99%.
Chuyển hóa: Daprodustat được chuyển hóa chủ yếu bởi CYP2C8 (95%) và một phần nhỏ qua enzyme CYP3A4 (5%).
Thải trừ: Sau 7 ngày uống Daprodustat, khoảng 74% được đào thải qua phân và 21% qua nước tiểu. Thời gian bán thải (T1/2) của Daprodustat nằm trong khoảng từ 1-4 giờ và độ thanh thải trung bình 18,9L/h.
2.4 Tác dụng phụ
Daprodustat có thể gây nhiều tác dụng không mong muốn nghiêm trọng bao gồm: khó thở, mệt mỏi, đau tức ngực, thở gấp, mất thị giác, chóng mặt, ngất xỉu, lú lẫn, tăng huyết áp, đau bụng, chóng mặt, quá mẫn
2.5 Triệu chứng quá liều
Nhức đầu và các vấn đề về tiêu hóa (buồn nôn) đều là các triệu chứng quá liều cấp tính khi sử dụng Daprodustat.
3.Cảnh báo và thận trọng
3.1 Tăng nguy cơ biến cố huyết khối động mạch và tĩnh mạch
Jesduvroq làm tăng nguy cơ xuất hiện cục máu đông trong động và tĩnh mạch, có thể gây tử vong, bao gồm nhồi máu cơ tim, đột quỵ, huyết khối tĩnh mạch và huyết khối tiếp cận mạch máu. Bệnh nhân mắc bệnh tim mạch hoặc mạch máu não có nguy cơ mắc các biến cố này cao hơn. Tránh sử dụng ở những bệnh nhân có tiền sử nhồi máu cơ tim, biến cố mạch máu não hoặc hội chứng mạch vành cấp tính trong vòng 3 tháng trước khi bắt đầu dùng thuốc. Bệnh nhân nên tìm tới các cơ sở y tế ngay khi có các dấu hiệu hoặc triệu chứng của nhồi máu cơ tim, đột quỵ, huyết khối tĩnh mạch hoặc huyết khối tiếp cận mạch máu để đánh giá và kiểm soát kịp thời
3.2 Nguy cơ nhập viện vì suy tim
Trong thử nghiệm ASCEND-D, tỷ lệ nhập viện vì suy tim là 7,5% ở bệnh nhân chạy thận nhân tạo thuốc. Xem xét tiền sử suy tim của bệnh nhân trước khi quyết định kê đơn và tư vấn cho bệnh nhân về các triệu chứng và dấu hiệu của suy tim và báo cáo ngay bất kỳ tình trạng xấu xảy ra
3.3 Tăng huyết áp
Trong thử nghiệm ASCEND-D, tình trạng tăng huyết áp trầm trọng hơn xảy ra ở 24% bệnh nhân dùng thuốc.
3.4 Xói mòn đường tiêu hóa
Trong thử nghiệm ASCEND-D, xói mòn dạ dày hoặc thực quản xảy ra ở 5,7% (2,5 trên 100 PY) bệnh nhân dùng thuốc. Cân nhắc nguy cơ này đặc biệt ở những bệnh nhân có nguy cơ cao bị xói mòn đường tiêu hóa, chẳng hạn như những người có tiền sử xói mòn đường tiêu hóa, bệnh loét dạ dày, sử dụng đồng thời các thuốc làm tăng nguy cơ xói mòn đường tiêu hóa, và những người hiện đang hút thuốc lá và uống rượu
4.Tương tác thuốc
Tương tác với chất ức chế CYP2C8: Chống chỉ định sử dụng đồng thời các chất ức chế CYP2C8 mạnh (ví dụ, gemfibrozil) với Jesduvroq do làm tăng đáng kể nồng độ Daprodustat
Tương tác với chất gây cảm ứng CYP2C8: Thuốc gây cảm ứng CYP2C8 (ví dụ, Rifampicin) có thể làm giảm nồng độ Daprodustat trong máu, điều này có thể dẫn đến mất hiệu quả.
5.Kết luận
Với lựa chọn thuốc uống ngoài các lựa chọn tiêm được FDA chấp thuận, những người trưởng thành mắc bệnh thận mãn tính có thêm phương án điều trị đường uống khác Daprodustat giúp cải thiện tình trạng thiếu máu
Leave a Reply